题目内容
【题目】粗盐中除含有泥沙等不溶性杂质外,还含有少量的MgCl2、CaCl2等可溶性杂质;为了得到较纯净的氯化钠,除去泥沙的“精盐”又作了如下处理(假定杂质只有MgCl2、CaCl2两种)注:反应中所加试剂均过量。
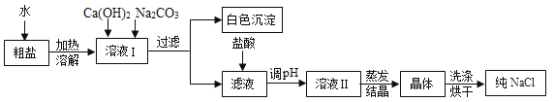
(1)实验中加入Na2CO3的目的是:_____。
(2)若实验过程中不考虑损耗,最终得到的NaCl固体的质量将_____(填“大于”“小于”或“等于”)原精盐中NaCl固体的质量。
(3)过滤后滤液中的杂质有哪些?_____。
【答案】除去粗盐中的氯化钙、反应生成的氯化钙和过量的氢氧化钙 大于 氢氧化钠和碳酸钠
【解析】
氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠。
(1)实验中加入Na2CO3的目的是:除去粗盐中的氯化钙、反应生成的氯化钙和过量的氢氧化钙。
(2)反应过程中有氯化钠生成,故若实验过程中不考虑损耗,最终得到的NaCl固体的质量将大于原精盐中NaCl固体的质量。
(3)过滤后液体中的杂质有反应生成的氢氧化钠和过量的碳酸钠。

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
【题目】某品牌矿泉水的标签上标明的矿泉水主要成分如下表所示,请根据下表回答下列问题:
水质主要成分(mgL﹣1) | |||
偏硅酸(H2SiO3) | 28.9~42.9 | 锶(Sr2+) | 0.01~0.32 |
碳酸氢根 | 173~205 | 钙 | 5~45 |
氯 | 1.0~8.0 | 钠 | 45~70 |
硫酸根 | 16.06~19.5 | 钾 | 0.5~2.0 |
镁 | 2.5~7.5 | pH | 7.8±0.5 |
(1)两个硫酸根离子的化学符号是_____。
(2)碳酸氢钙的化学式是_____。
(3)用结构示意图表示C1﹣的核外电子排布:_____。
(4)偏硅酸中硅元素的化合价是_____。