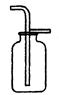
题目内容
为控制大气中“温室效应”(CO2、CH4)气体的排放量,“低碳”正成为人们的共识。
(1)近几十年来大气中二氧化碳含量不断上升的主要原因是 。
(2)生活中燃烧等物质的量的碳、一氧化碳、甲烷,最终排放出的二氧化碳的量 (选填编号)
| A.一样多 | B.碳多 | C.一氧化碳多 | D.甲烷多 |
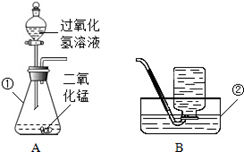
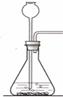
(4)实验室制取二氧化碳,采用的实验原理用化学方程式表示为 ;
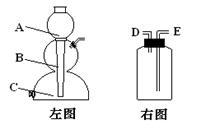
若用左图制取CO2则碳酸钙固体应该放置的位置是 ,若用右图收集CO2则气体进入的导管口应该是 (以上均用图中英文编号填写)。
(5)实验室利用澄清石灰水检验CO2时发生的化学方程式为 。
(1)燃烧煤炭、石油等矿物燃料
(2)A
(3)2Mg+CO2 2MgO+C Mg
2MgO+C Mg
(4)CaCO3+2HCl→CaCl2+H2O+CO2↑ B )E
(5)CO2+Ca(OH)2→CaCO3↓+H2O
解析试题分析:近几十年来由于燃烧煤炭、石油等矿物燃料燃料量增大,大气中二氧化碳含量不断上升;由于相同物质的量的的碳、一氧化碳和甲烷中含有相同物质的量的碳,根据质量守恒定律以上三种物质中的碳完全燃烧后都生成了二氧化碳,所以它们完全燃烧后都生成了相同物质的量的二氧化碳;镁在二氧化碳中燃烧生成氧化镁和碳,其中镁夺走了二氧化碳中的氧,发生了氧化反应是还原剂;实验室制是以石灰石和稀盐酸为原料制取二氧化碳的,该反应的生成物是氯化钙、水和二氧化碳,应根据以上信息书写化学方程式;若用启普发生器制取二氧化碳等气体,固体应放在B处;由于二氧化碳的密度比空气大若用右图装置收集气体,应从E端进入;二氧化碳与澄清石灰水中的溶质氢氧化钙发生化学反应生成碳酸钙沉淀和水,根据这些信息书写化学方程式。
考点:二氧化碳的来源、检验,化学方程式的书写和计算,氧气-还原反应。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在下列实验方案中,均选用 BaCl2 溶液做试剂,其中不合理的是
| A.除去稀盐酸中混有的少量稀硫酸 | B.区分 CO2气体和 HCl 气体 |
| C.除去 NaCl 中混有的杂质 Na2CO3 | D.鉴别 AgNO3溶液和 NaCl 溶液 |
下列实验方法、现象、结论均正确的是( )
| 选项 | 实验方法 | 现象 | 结论 |
| A | 用pH试纸测肥皂液的酸碱性 | 试纸变黄(pH<7) | 肥皂液呈酸性 |
| B | 铜丝放入稀硝酸中 | 有气泡产生 | 铜可以置换出酸中的氢气 |
| C | 燃烧法测定纤维种类 | 烧毛发的气味 | 该纤维是棉纤维 |
| D | 蓝墨水滴入盛有水的水杯中 | 一段时间后整杯水变蓝 | 分子是不断运动的 |
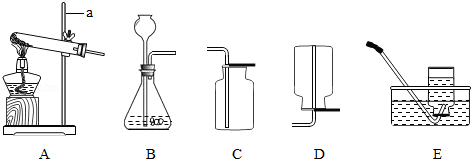

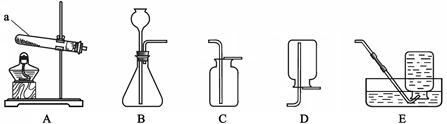
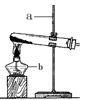
 2H2O + O2↑,在实验室利用此反应制取氧气时,应选用的气体发生装置是 。
2H2O + O2↑,在实验室利用此反应制取氧气时,应选用的气体发生装置是 。