题目内容
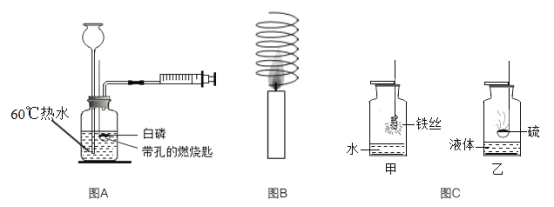
【题目】锌锰电池(俗称干电池)在生活中的用量很大,其构造如图甲所示。
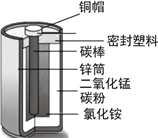
(1)图示物品所使用的主要材料属于金属材料的是__________(填字母序号)。
A.密封塑料 B.铜帽 C.二氧化锰 D.锌筒
(2)回收废旧电池中的铜帽(铜锌合金)和锌筒可得到铜锌渣,经检测铜锌渣中约含Zn 18%、Cu 50%、CuO 25%,其余为杂质。处理铜锌渣可制取铜和硫酸锌溶液,其主要流程如图(杂质不溶于水、不参与反应):
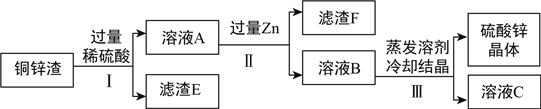
写出步骤Ⅰ中反应的化学方程式为__________________;_________________。
②步骤Ⅱ中加入过量Zn的目的是除去过量的稀硫酸和______________________________。
③下列说法正确的是__________(填字母序号)
A.溶液B与溶液C中所含溶质相同 B.步骤Ⅰ、Ⅱ中的操作均包含过滤
C.过程Ⅱ中发生的反应均为置换反应 D.滤渣F是纯的铜
【答案】 BD Zn+H2SO4=ZnSO4+H2↑ CuO+H2SO4=CuSO4+H2O CuSO4 ABC
【解析】(1)铜帽和锌铜属于金属材料,故选BD;
(2)①Zn、CuO都可与稀H2SO4反应;Cu不可与H2SO4反应;故反应方程式为①Zn+H2SO4=ZnSO4+H2↑;CuO+H2SO4=CuSO4+H2O;
②加入Zn是为了除去适量的稀H2SO4和CuSO4;
③A.溶液B和C中的溶质均为ZnSO4,正确;
B.Ⅰ、Ⅱ操作中都有固液分离的操作,即为过滤,正确;
C.Ⅱ中发生的反应另Zn和稀H2SO4,Zn和CuSO4反应后,均为置换,正确;
D.F中有Zn、Cu,不是纯的铜,错误。故选ABC;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】甲、乙、丙三种物质的转化关系如图所示(“→、←”表示反应一步实现,部分物质和反应条件已略去)。下列选项不能实现图示转化的是
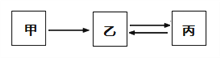
选项 | 甲 | 乙 | 丙 |
A | H2SO4 | H2 | H2O |
B | C | CO | CO2 |
C | Fe2O3 | Fe | Fe3O4 |
D | CaO | Ca(OH)2 | CaCO3 |
A. A B. B C. C D. D
【题目】将一定量的X和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | X | 氧气 | 水 | 二氧化碳 |
反应前质量/g | 4.6 | 10.6 | 1.6 | 1.2 |
反应后质量/g | a | 1.0 | 7.0 | 10.0 |
下列判断不正确的是
A. 表中a的值为0 B. 物质X一定是有机物
C. 反应中水和氧气的质量比是9:16 D. 物质X不含氧元素