题目内容
【题目】请根据以下三个实验回答问题:
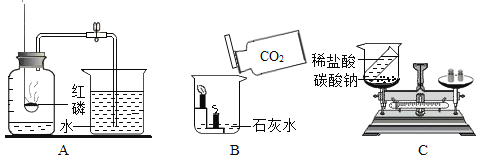
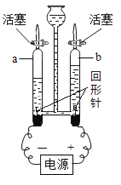
(1)A实验的目的是什么?_______
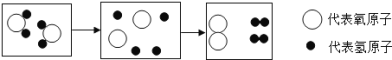
(2)B实验说明二氧化碳具有哪些性质?(至少答出两点)______
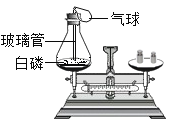
(3)为什么用C实验无法验证质量守恒定律?_______
【答案】测定空气中氧气的含量 密度比空气大、不燃烧、也不支持燃烧、能与石灰水反应等其中两点 未在密闭的容器内进行,反应生成的气体逸散到空气中
【解析】
(1) A实验的目的是根据反应前后压强差原理,测定空气中氧气的含量,故填写:测定空气中氧气的含量;
(2) B实验观察到的实验现象是:澄清石灰水变浑浊,蜡烛由低到高熄灭,说明二氧化碳密度比空气大、不燃烧、也不支持燃烧、能与石灰水反应,故填写:密度比空气大、不燃烧、也不支持燃烧、能与石灰水反应等其中两点;
(3) C实验未在密闭的容器内进行,反应生成的气体逸散到空气中,故填写:未在密闭的容器内进行,反应生成的气体逸散到空气中。

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案【题目】定量研究对于化学科学发展有重大作用,因此我们应该掌握好有关质量守恒定律的相关知识。
(1)在化学变化前后一定不变的是_________(填序号)。
①原子数目 ②分子种类 ③原子种类 ④元素种类 ⑤物质种类 ⑥物质的总质量
(2)自然界中绿色植物光合作用的表达式如下:CO2 + H2O 淀粉 + O2.从化学反应前后元素种类变化情况的角度分析可知:淀粉中一定含有_____________元素。
淀粉 + O2.从化学反应前后元素种类变化情况的角度分析可知:淀粉中一定含有_____________元素。
(3)在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物 质 | A | B | C | D |
反应前质量∕g | 2 | 24.5 | 4 | 8 |
反应后质量∕g | 16.9 | 0 | 13.6 | X |
表中X=________,在反应中D这种物质可能作________使用。容器内发生的反应的基本类型是_______________(选填:化合反应或分解反应)。若B物质为氯酸钾请写出容器内所发生的反应的化学方程式___________________。