题目内容
【题目】小明同学在完成实验室制取CO2后,对回收的盐酸和CaCl2混合溶液(不考虑其它杂质)进行以下实验:取200g该溶液于烧杯中,向其中滴加溶质质量分数为10.6%的Na2CO3溶液,滴入Na2CO3溶液与生成沉淀的质量关系如图所示。
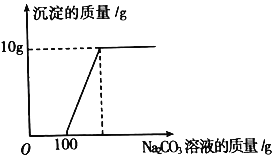
(1)生成沉淀的质量为_____g?
(2)回收液中HCl的质量分数是多少_____?
(3)当Na2CO3溶液与CaCl2溶液恰好完全反应时,溶液中溶质的质量是多少_____?
【答案】10 3.65% 23.4g
【解析】
(1)由图象可知,生成沉淀的质量为10g;
(2)由图中数据可知与HCl反应的碳酸钠溶液的质量为100g。
解:根据题意跟盐酸反应的碳酸钠质量为:100g×10.6%=10.6g。
设回收液中HCl的质量分数是x、生成氯化钠的质量为y。
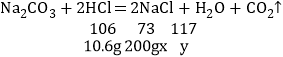
![]()
解得x=3.65%
![]()
解得y=11.7g
⑶设碳酸钠与氯化钙反应生成的氯化钠的质量为m。
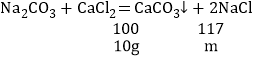
![]()
解得m=11.7g
当Na2CO3溶液与CaCl2溶液恰好完全反应时,溶液中溶质的质量:11.7g+11.7g=23.4g。
答:(1)反应中生成沉淀的质量为10g;(2)回收液中HCl的质量分数是3.65%;(3)当Na2CO3溶液与CaCl2溶液恰好完全反应时,溶液中溶质的质量是23.4g。

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
【题目】将一定量的丙醇(C3H8O)和氧气置于一个密封的容器中引燃,测得反应前后各物质的质量如表。下列说法错误的是( )
物质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 6.0 | 14.8 | 0 | 0.4 | 0 |
反应后质量/g | 0 | 2 | 7.2 | 9.2 | a |
A. 表中a的值为2.8
B. 参加反应的氧气和生成二氧化碳的质量比为16:11
C. X中一定含碳元素、氧元素
D. 该反应属于分解反应