题目内容
【题目】某探究小组为了探究镁、铝、铜的金属活动性强弱,设计了以下实验探究方案。
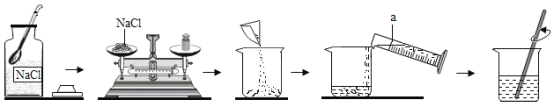
[实验探究1]将大小一样且均未打磨的镁、铝、铜片分别放人等质量的溶质质量分数相同的稀盐酸中。
[实验现象]镁片表面很快产生大量气泡,铝表面过一段时间后才产生较少气泡,铜不反应。
[结论]镁、铝、铜的金属活动性由强到弱的顺序为_____。
(1)一段时间后,铝片表面才产生较少气泡的原因是_____(用化学方程式表示)。
(2)有同学提出疑问:镁、铝、铜片均未打磨,会影响反应现象,那么镁、铝、铜片有必要打磨吗?_____,打磨的目的是_____。
[实验探究2]取打磨过的镁片、铝片分别插人盛有硫酸铜溶液的试管中。镁片、铝片表面都有红色疏松的物质析出,硫酸铜溶液颜色变浅。据此可以探究出三者的金属活动性强弱。
(3)写出铝与硫酸铜溶液反应的化学方程式:_____。
[拓展探究]细心的同学发现,将打磨过的镁片插人硫酸铜溶液中时,镁片表面除了有红色疏松的物质析出,还有气泡产生。为什么会有气泡产生呢?
[查阅资料]在硫酸铜溶液中,由于铜离子的水解作用,溶液显酸性。硫酸铜溶液的浓度越大,铜离子的水解作用越强。
(4)试写出镁片与硫酸铜溶液反应产生气泡的化学方程式:_____。
(5)试设计实验探究硫酸铜溶液的浓度与铜离子的水解作用的关系:_____。
【答案】镁>铝>铜 ![]() 有必要 除去金属表面的氧化膜及其他杂质
有必要 除去金属表面的氧化膜及其他杂质 ![]()
![]() 分别取10mL质量分数为5%和10%的硫酸铜溶液于试管中,放入大小一样且均打磨过的镁片,若放入质量分数为10%的硫酸铜溶液中的镁片产生气泡的速度明显快于质量分数为5%的硫酸铜溶液,则硫酸铜溶液的浓度越大,铜离子的水解作用越强(合理即可)
分别取10mL质量分数为5%和10%的硫酸铜溶液于试管中,放入大小一样且均打磨过的镁片,若放入质量分数为10%的硫酸铜溶液中的镁片产生气泡的速度明显快于质量分数为5%的硫酸铜溶液,则硫酸铜溶液的浓度越大,铜离子的水解作用越强(合理即可)
【解析】
[结论]根据金属与酸反应的剧烈程度,可知镁、铝、铜的金属活动性由强到弱的顺序为镁>铝>铜。
(1)铝表面有一层致密的氧化铝薄膜,氧化铝先与稀盐酸反应生成氯化铝和水,其化学方程式为![]() 。
。
(2)镁、铝、铜片有必要打磨,打磨可以除去金属表面的氧化膜及其他杂质,有利于金属直接与稀盐酸接触而发生发应。
(3)铝与硫酸铜溶液反应生成硫酸铝和铜,其化学方程式![]() 。
。
[查阅资料]在硫酸铜溶液中,由于铜离子的水解作用,溶液显酸性。硫酸铜溶液的浓度越大,铜离子的水解作用越强。
(4)在硫酸铜溶液中,由于铜离子的水解作用,溶液显酸性,则镁片与硫酸铜溶液反应实际上与稀硫酸也发生了反应产生氢气,其化学方程式![]() 。
。
(5)若想探究硫酸铜溶液的浓度与铜离子的水解作用的关系,可取不同浓度的硫酸铜溶液,与镁片反应,看产生气泡的速度即可,实验中要注意控制变量,具体步骤为:分别取10mL质量分数为5%和10%的硫酸铜溶液于试管中,放入大小一样且均打磨过的镁片,若放入质量分数为10%的硫酸铜溶液中的镁片产生气泡的速度明显快于质量分数为5%的硫酸铜溶液,则硫酸铜溶液的浓度越大,铜离子的水解作用越强。

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案【题目】CaO和NaOH固体的混合物,俗称“碱石灰”,实验室常用作干燥剂。碱石灰在空气中容易吸收空气中的水和二氧化碳变质。某实验小组为确定一瓶久置的碱石灰样品的成分,设计了如图所示的实验流程;
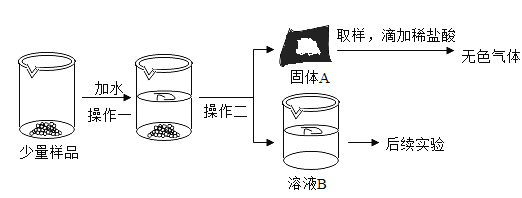
请你参与探究过程:
(1)固体A中一定含有_________。
(2)溶液B成分的探究:
(查阅资料)①Ca(OH)2、Na2CO3溶于水无明显的温度变化;② CaCl2溶液呈中性。
(猜想)溶液B中溶质可能为:①NaOH ②Na2CO3 ③NaOH和Na2CO3 ④Ca(OH)2和______(填化学式)。
(设计方案并进行实验)甲、乙同学分别设计如下方案并进行探究:
甲同学:取少量溶液B于试管中,滴加足量的稀盐酸,产生大量气泡,则溶液B中的溶质是Na2CO3;
乙同学:取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,则溶液B中的溶质一定含有NaOH。
(反思与评价)丙同学认真分析上述两位同学的实验,认为他们的结论均有不足之处,乙同学实验不足之处在于______________________________________。
为进一步确认溶液B中是否含NaOH,他做了如下实验:
实验步骤 | 实验现象 | 实验结论 |
①取少量溶液B于试管中,加入足量的________溶液 ②过滤,在滤液中滴加酚酞试液 | ①生白色沉淀 ②_______ | 猜想③正确 |
(3)实验过程中,同学们发现向样品中加水时还放出大量的热。综合以上探究,下列对样品成分分析正确的是______(填序号)。
A 一定有CaCO3 B 一定有NaOH C 一定有Na2CO3 D 可能有CaO