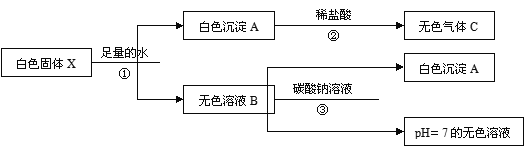
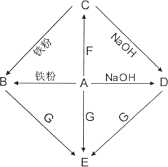
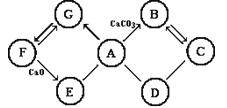
题目内容
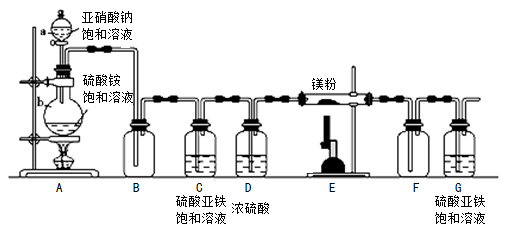
【题目】(7分)甲、乙两组同学分别利用下图所示装置,测量含少量氯化钠的纯碱样品的纯度。两组实验中,锥形瓶内都盛有m g的纯碱样品;分液漏斗中,甲组盛有稀硫酸,乙组盛有浓盐酸。(装置气密性良好,实验前活塞a、b均处于关闭状态。)
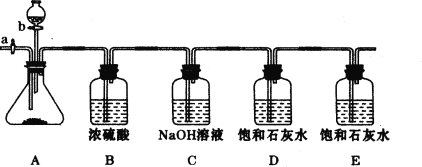
主要步骤及观察到的现象如下:
I、打开活塞a,通入氮气一会儿再关闭活塞a,称量装置C、D、E的质量。
Ⅱ、打开活塞b。甲组同学滴加足量的稀硫酸;乙组同学滴加足量的浓盐酸后,关闭活塞b。
Ⅲ、锥形瓶中不再产生气泡时打开活塞a,通人氮气一会儿再关闭活塞a。甲组同学观察,到装置D、E中均无明显变化;乙组同学观察到装置D中出现明显的浑浊,装置E中无明显变化。
Ⅳ、甲组同学实验后测得装置C的质量增加了n g。
请回答下列问题:
(1)两组同学都使用了浓硫酸,其作用是________________________________;
(2)写出甲组同学装置A中反应的化学方程式________________________________;
(3)甲组同学所测定的纯碱样品的质量分数=__________________________________;
(4)乙组有同学提议:利用本组测得装置C和装置D增加的总质量计算,就能得到与甲组同样的结果。你认为该看法___________________(填“正确”或“不正确”),理由是____________________________。
【答案】(1)干燥二氧化碳_;
(2)Na2CO3+H2SO4==Na2SO4+CO2↑+H2O;
(3)![]()
(4)不正确,CD增加的质量是吸收的氯化氢和二氧化碳的质量的总和。
【解析】
试题分析:(1)浓硫酸有吸水性,常做气体的干燥剂 ;
(2)碳酸钠和硫酸反应生成硫酸钠、二氧化碳、和水;
(3)设样品中碳酸钠的质量是x
Na2CO3+H2SO4==Na2SO4 + CO2↑+H2O
106 44
x ng
106/x==44/ng x=![]()
样品中碳酸钠的纯度==![]() ÷mg×100%
÷mg×100%
(4)浓盐酸有很强的挥发,挥发出的溶质氯化氢和生成的二氧化碳都会被氢氧化钠溶液、石灰水吸收

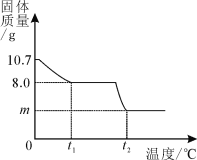
【题目】(4分)(1)下图是a、b、c三种物质溶解度曲线,a与c溶解度曲线相交于P点。

据图回答:①P点的含义是 。
②t2℃时30g a物质加入到50g水中不断搅拌,形成溶液质量是 g。
③将t2℃时a、b、c三种物质饱和溶液的温度降到t1 ℃时,三种溶液中溶质的质量分数由大到小的顺序排列是 。
(2)KNO3和KCl在不同温度时的溶解度如下表所示:
/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
由表中数据分析可知,KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值最小范围是 。