题目内容
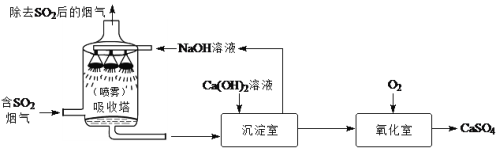
【题目】下面是五种粒子的结构示意图,下列说法错误的是
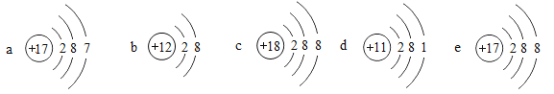
A.图中表示阴离子的是e
B.图中表示阳离子的是a
C.图中粒子共代表的是四种元素
D.若d、a的元素符号分别为X、Y,那么它们形成的化合物化学式为XY
【答案】B
【解析】
根据粒子结构示意图判断粒子种类的方法是:原子中,质子数=核外电子数;阳离子中,质子数>核外电子数;阴离子中,质子数﹤核外电子数。
A、e中质子数是17,核外电子数是18,质子数﹤核外电子数,因此e是阴离子,选项A正确;
B、a粒子中,质子数=核外电子数,表示的是原子,b粒子中质子数>核外电子数,表示的是阳离子,选项B不正确;
C、元素是质子数相同的一类原子的总称,质子数相同的原子和简单离子(带电的原子)属于同种元素,因此a和e属于同种元素,所以图中五种粒子共代表的是四种元素,选项C正确;
D、d表示的是钠原子,a表示的是氯原子。钠原子最外层是一个电子容易失去,变成带一个单位正电荷的Na+,显+1价,氯原子最外层是七个电子容易得到一个电子,变成带一个单位负电荷的Cl-,显-1价,形成的化合物化学式是NaCl。因此若d、a的元素符号分别为X、Y,那么它们形成的化合物化学式为XY,选项D正确。故选B。

 字词句篇与同步作文达标系列答案
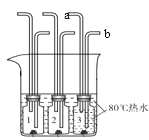
字词句篇与同步作文达标系列答案【题目】某化学兴趣小组在一次实验中进行如图所示的实验:

此时观察到U形管左右两侧产生的现象是不同的;实验后,小组同学充分振荡U形管。发现管内仍有白色固体残留。将固体分离后,同学们对滤液成分产生浓厚的兴趣,于是进行了进一步的探究活动
(1)(提出问题)滤液中可能含有哪些溶质?
(猜想与假设)猜想一:溶质为NaCl
猜想二:溶质为NaCl和BaCl2
猜想三:溶质为NaCl、BaCl2和HCl
你认为以上猜想_____不合理;理由是_____(请用化学方程式表示);请写出你的猜想_____。
(2)(实验探究)小红为了验证滤液成分,取滤液于试管中,向其中滴加少量的硫酸钠溶液,观察到无明显现象。由此得出结论:猜想一成立。小刚认为小红的结论是否严密_____(填“严密”或“不严”)。
为了验证你的猜想,请填写下表:
实验操作 | 实验现象 | 实验结论 |
取滤液适量于试管中,向其中滴加适量_____溶液 | 溶液由无色变为红色 | 你的猜想成立 |
(3)(归纳与总结)通过上述实验,我们能够总结出:在确定化学反应后所得溶液溶质成分时,除了考虑生成物外,还需要考虑_____。