题目内容
 某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:(1)小红同学从某一欠收农田里取回一份土壤样品,如果检测结果呈酸性,从经济和可行方面考虑,那么要改良此土壤的酸性,应向农田里施加
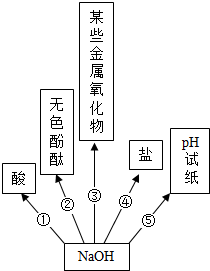
(2)小红同学用如图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).
Ⅰ.为了验证反应?,小红将无色酚酞试液滴入NaOH溶液中,溶液由无色变成
Ⅱ.依据反应?说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:
Ⅲ.为了验证反应④能够发生,你选择的物质是
A.Na2CO3 B.HCl C.FeCl3 D.Ba(OH)2
(3)请你设计一个实验除去FeCl2溶液中少量的CuCl2:
| 实验操作 | 化学方程式 |
| ① | CuCl2+Fe═Cu+FeCl2 |
| ②过滤 |
考点:碱的化学性质,常见碱的特性和用途,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:(1)氢氧化钙显碱性,能和显酸性的物质发生化学反应;
(2)氢氧化钠溶液显碱性,能使酚酞试液变红色;
氢氧化钠溶液能够吸收空气中的二氧化碳,并且能和二氧化碳反应生成碳酸钠和水;
氢氧化钠能和氯化铁反应生成红褐色沉淀氢氧化铁和氯化钠;
(3)铁比铜活泼,能和氯化铜反应生成氯化亚铁和铜.
(2)氢氧化钠溶液显碱性,能使酚酞试液变红色;
氢氧化钠溶液能够吸收空气中的二氧化碳,并且能和二氧化碳反应生成碳酸钠和水;
氢氧化钠能和氯化铁反应生成红褐色沉淀氢氧化铁和氯化钠;
(3)铁比铜活泼,能和氯化铜反应生成氯化亚铁和铜.
解答:解:(1)从经济和可行方面考虑,那么要改良此土壤的酸性,应向农田里施加氢氧化钙,氢氧化钙的化学式是Ca(OH)2.
故填:Ca(OH)2.
(2)Ⅰ.为了验证反应?,小红将无色酚酞试液滴入NaOH溶液中,溶液由无色变成红色.
故填:红色.
Ⅱ.氢氧化钠和二氧化碳反应的化学方程式为:
依据反应?说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:2NaOH+CO2═Na2CO3+H2O.
故填:2NaOH+CO2═Na2CO3+H2O.
Ⅲ.碳酸钠属于盐,不能和氢氧化钠反应;
盐酸和氢氧化钡不属于盐;
氯化铁能和氢氧化钠反应生成红褐色沉淀氢氧化铁和氯化钠,为了验证反应④能够发生,应该选择的物质是氯化铁.
故填:C.
(3)向溶液中加入过量的铁粉,充分反应后过滤,可以除去FeCl2溶液中少量的CuCl2.
故填:向溶液中加入过量的铁粉.
故填:Ca(OH)2.
(2)Ⅰ.为了验证反应?,小红将无色酚酞试液滴入NaOH溶液中,溶液由无色变成红色.
故填:红色.
Ⅱ.氢氧化钠和二氧化碳反应的化学方程式为:
依据反应?说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:2NaOH+CO2═Na2CO3+H2O.
故填:2NaOH+CO2═Na2CO3+H2O.
Ⅲ.碳酸钠属于盐,不能和氢氧化钠反应;
盐酸和氢氧化钡不属于盐;
氯化铁能和氢氧化钠反应生成红褐色沉淀氢氧化铁和氯化钠,为了验证反应④能够发生,应该选择的物质是氯化铁.
故填:C.
(3)向溶液中加入过量的铁粉,充分反应后过滤,可以除去FeCl2溶液中少量的CuCl2.
故填:向溶液中加入过量的铁粉.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
下列各组物质中,前者属于单质,后者属于氧化物的是( )
| A、液氧、蒸馏水 |
| B、稀有气体、硬水 |
| C、氮气、大理石 |
| D、高锰酸钾、洁净的空气 |