题目内容
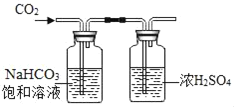
【题目】现有一包固体的混合物,可能含有Na2SO4、Na2CO3、NaCl、NaNO3中的两种或两种以上。小红想知道混合物的成分,便和实验小组同学共同设计以下实验。
A的浓溶液常用作干燥剂。
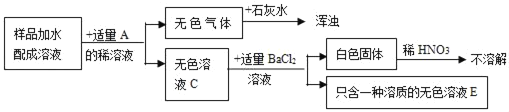
(1)写出B、D的化学式B_____;D_____
(2)向样品中加入A的稀溶液,反应的化学方程式:_____
(3)实验结束了,小红得知混合物的组成可能是(写化学式)(可不填满)
①_____;②_____;③_____;④_____。
【答案】CO2 BaSO4 Na2CO3 +H2SO4=Na2SO4+H2O+CO2↑ Na2CO3、Na2SO4 Na2CO3、NaCl Na2CO3、Na2SO4 NaCl
【解析】
碳酸盐和酸反应会生成二氧化碳,二氧化碳能使石灰水变浑浊,硫酸钠和氯化钡反应生成不溶于水的硫酸钡沉淀,所以
样品中加入酸生成的无色气体能使澄清石灰水变浑浊,所以样品中一定含有碳酸钠;无色溶液C中加入适量的氯化钡,生成的白色沉淀不溶于硝酸,所以样品中一定含有硫酸钠,氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,E溶液中含有一种溶质,所以样品中一定不含硝酸钠,所以
A的浓溶液常用作干燥剂,所以A是稀硫酸,
(1)B、D的化学式B是CO2,D是BaSO4;
(2)向样品中加入A的稀溶液的反应是碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,化学方程式为:Na2CO3 +H2SO4=Na2SO4+H2O+CO2↑;
(3)实验结束了,小红得知混合物的组成可能是:①Na2CO3、Na2SO4;②Na2CO3、NaCl;③Na2CO3、Na2SO4、NaCl。
故答案为:(1)CO2,BaSO4;(2)Na2CO3 +H2SO4=Na2SO4+H2O+CO2↑;(3)Na2CO3、Na2SO4; Na2CO3、NaCl; Na2CO3、Na2SO4、NaCl。

【题目】将一定量的丙醇(C3H8O)和氧气置于一个封闭的容器中引燃,其反应的化学方程式为: aC3H8O+bO2![]() cCO2+dH2O+eX,测得反应前后各物质的质量如下表:
cCO2+dH2O+eX,测得反应前后各物质的质量如下表:
物质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 6.0 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 8.8 | x |
下列判断正确的是( )
A. 表中x的值为1.8B. x可能是该反应的催化剂
C. X可能为甲烷D. 方程式中a:b=1:4