题目内容
已知某合金粉末除铝外,还含有铁、铜中的一种或两种.某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.[查阅资料]
铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2易溶于水);Fe、Cu不与氢氧化钠溶液反应.
[猜想]
猜想1:该合金粉末中除铝外,还含有铁、铜.
猜想2:该合金粉末中除铝外,还含有______(填名称).
猜想3:该合金粉末中除铝外,还含有铁.
[实验探究]
下列实验仅供选择的试剂:10% 盐酸、30% NaOH溶液.
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的______,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有______. |
| ②取步骤①所得滤渣,加过量的______,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有______. |
猜想1成立.
[实验反思]
一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.
[拓展延伸]
铜和稀硫酸在通常情况下不反应.但在特定条件下(如电解),铜和稀硫酸可以发生置换反应,并生成氢气.请写出此反应的化学方程式______ CuSO4+H2↑
【答案】分析:已知某合金粉末除铝外,还含有铁、铜中的一种或两种,因此做出的猜想有三种:该合金粉末中除铝外,还含有铁、铜;该合金粉末中除铝外,还含有铜;该合金粉末中除铝外,还含有铁.因为铝和铁都能与盐酸反应,铜与盐酸不反应,铝与氢氧化钠溶液能反应;由实验现象:滤渣部分溶解,并有气体放出,溶液呈浅绿色可以判断:①中加入的是30% NaOH溶液,粉末部分溶解,并有气体放出,说明合金中一定含有铝;②中加入的是10% 盐酸,由现象知:合金中一定含有铜和铁.铜和硫酸在电解的条件下生成硫酸铜和氢气;易拉罐开始时变瘪的原因是二氧化碳与氢氧化钠反应,压强减小;易拉罐重新鼓起的原因是:铝与氢氧化钠溶液反应生成了氢气的缘故.
解答:解:(1)做出的猜想有三种:该合金粉末中除铝外,还含有铁、铜;该合金粉末中除铝外,还含有铜;该合金粉末中除铝外,还含有铁;故答案为:铜;
(2)因为铝和铁都能与盐酸反应,铜与盐酸不反应,铝与氢氧化钠溶液能反应;由实验现象:滤渣部分溶解,并有气体放出,溶液呈浅绿色可以判断:①中加入的是30% NaOH溶液,粉末部分溶解,并有气体放出,说明合金中一定含有铝;②中加入的是10% 盐酸,由现象知:合金中一定含有铜和铁.故答案为:①30% NaOH溶液;铝;②10% 盐酸;铜和铁
(3)铜和硫酸在电解的条件下生成硫酸铜和氢气,故答案为:Cu+H2SO4 CuSO4+H2↑
CuSO4+H2↑
(4)易拉罐开始时变瘪的原因是二氧化碳与氢氧化钠反应,压强减小;易拉罐重新鼓起的原因是:铝与氢氧化钠溶液反应生成了氢气,故答案为:CO2+2NaOH=Na2CO3+H2O;氢气
点评:实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.有关实验方案的设计和对实验方案的评价是中考的热点之一,要好好把握.
解答:解:(1)做出的猜想有三种:该合金粉末中除铝外,还含有铁、铜;该合金粉末中除铝外,还含有铜;该合金粉末中除铝外,还含有铁;故答案为:铜;
(2)因为铝和铁都能与盐酸反应,铜与盐酸不反应,铝与氢氧化钠溶液能反应;由实验现象:滤渣部分溶解,并有气体放出,溶液呈浅绿色可以判断:①中加入的是30% NaOH溶液,粉末部分溶解,并有气体放出,说明合金中一定含有铝;②中加入的是10% 盐酸,由现象知:合金中一定含有铜和铁.故答案为:①30% NaOH溶液;铝;②10% 盐酸;铜和铁
(3)铜和硫酸在电解的条件下生成硫酸铜和氢气,故答案为:Cu+H2SO4
 CuSO4+H2↑
CuSO4+H2↑(4)易拉罐开始时变瘪的原因是二氧化碳与氢氧化钠反应,压强减小;易拉罐重新鼓起的原因是:铝与氢氧化钠溶液反应生成了氢气,故答案为:CO2+2NaOH=Na2CO3+H2O;氢气
点评:实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.有关实验方案的设计和对实验方案的评价是中考的热点之一,要好好把握.

练习册系列答案
相关题目


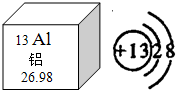 铝被称为“年轻的金属”,据世界化学史记载,金属铝是在1825年才被英国化学家戴维制得.今天,铝已经进入了我们生活的每一个角落.
铝被称为“年轻的金属”,据世界化学史记载,金属铝是在1825年才被英国化学家戴维制得.今天,铝已经进入了我们生活的每一个角落.