题目内容
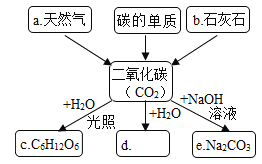
【题目】小可同学对前几个单元所学物质及其转化关系进行了归纳,如图所示(部分生成已略去),据图回答:
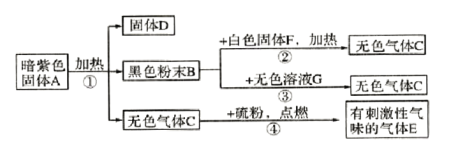
(1)写出物质A的名称:_______________;
(2)写出反应②的文字表达式:______________;
(3)黑色粉末B在反应②和③中都起_____________作用。
【答案】高锰酸钾 氯酸钾![]() 氯化钾+氧气 催化
氯化钾+氧气 催化
【解析】
根据反应④的反应条件可知,无色气体C是氧气,硫在氧气中燃烧生成有刺激性气味的二氧化硫,E是二氧化硫;①②③都生成氧气,生成氧气的反应有暗紫色固体高锰酸钾加热制取氧气、白色固体氯酸钾和黑色固体二氧化锰加热制取氧气、无色液体过氧化氢和黑色固体二氧化锰制取氧气,所以反应①②③依次为暗紫色固体高锰酸钾加热制取氧气、白色固体氯酸钾和黑色固体二氧化锰加热制取氧气、无色液体过氧化氢和黑色固体二氧化锰制取氧气。
(1)物质A的名称是高锰酸钾;
(2)反应②是白色固体氯酸钾和黑色固体二氧化锰加热制取氧气,文字表达式:氯酸钾![]() 氯化钾+氧气
氯化钾+氧气
(3)黑色粉末B是二氧化锰,二氧化锰在反应②和③中做催化剂,都起催化作用。

【题目】在化学学习过程中,我们常常需要通过科学探究来认识物质,研究物质的化学变化,请你一起参与下列实验探究。
(探究Ⅰ:以过氧化氢分解为研究对象进行实验,探究影响化学反应速率的因素)
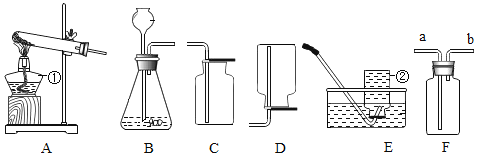
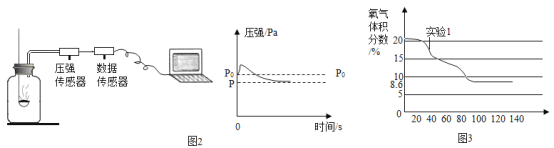
三个小组均可采用如图装置进行实验,记录收集10mL氧气的时间,实验室可供选择的试剂有:2.5%、5%、10%三种浓度的H2O2溶液、MnO2、CuO、红砖粉末。
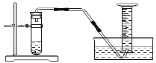
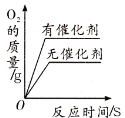
A组:探究催化剂对化学反应速率的影响
取5mL10%H2O2溶液,三次实验分别加入0.5gMnO2、红砖粉末、CuO进行实验,记录数据如下:
试剂 | MnO2 | 红砖粉末 | CuO |
t/s | 10 | 60 | 20 |
由此可出结论:MnO2、CuO对H2O2分解有催化作用,红砖粉末无催化作用,某同学对该结论提出疑问。
补充对比实验,操作为_____________________。
结果:长时间(大于100s),收集到很少量气体。
更正结论:红砖粉末有催化作用,三者中MnO2催化效率最高。
B组:探究浓度对化学反应速率的影响
甲同学:取10mL5%H2O2溶液,加入0.5gMnO2为催化剂,进行实验,记录时间t1。
乙同学:取10mL2.5%H2O2溶液,加入0.5g CuO为催化剂,进行实验,记录时间t2。
实验结果t1______t2(填“>”或“<”)。
结论:浓度越大,反应速率越快。
丙同学:对实验设计提出疑问,并补充实验___________________,
记录时间t3,且t1<t3<t2。
更正结论为:当催化剂种类及质量相同时,反应物浓度越大,____________。
C组:探究__________对化学反应速率的影响。
取10mL5%H2O2溶液和0.5gCuO为催化剂进行实验,两次实验分别将试管置于冰水浴和50℃热水浴记录时间t4、t5,且t4>t5。
结论:当反应物浓度和催化剂相同时,_____________________。
综上所述:为了研究某一因素对化学反应速率的影响,必须只允许有一个变量,其他量必须相同。
(探究Ⅱ:二氧化碳的性质探究)
铁丝(含碳量0.69%)在氧气中燃烧,铁丝燃烧时火星四射,经研究表明产生火星四射现象的原因,可能是同时生成了某种气体,推测该气体是___________(填名称)。
查阅资料:①CO2和SO2溶于水后具有相似的化学性质②硫是淡黄色固体
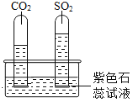
实验一:水槽中滴入紫色石蕊,将收集满两种气体的试管同时倒立于其中,片刻后实验现象如图所示,说明相同条件下的溶解性:SO2_____(填“>”或“<”)CO2,试管内溶液变成____________色。
实验二:已知镁条可以在CO2中剧烈燃烧,反应为:Mg+CO2![]() MgO+C,试推测镁条在SO2中燃烧的现象为:剧烈燃烧、放出热量________________。
MgO+C,试推测镁条在SO2中燃烧的现象为:剧烈燃烧、放出热量________________。