题目内容
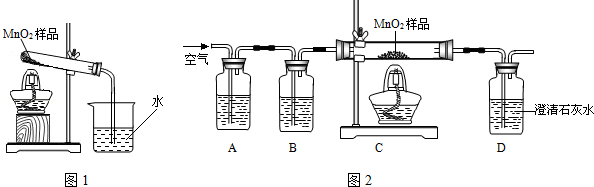
同学们对美术组的环保石头纸(主要成分为碳酸钙,加入适量聚乙烯和少量胶合剂)展开探究:
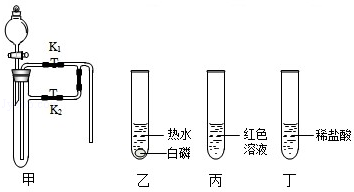
[拓展实验一] 探究影响石头纸与盐酸反应快慢的因素
(1)甲、乙两同学设计实验如下:
[拓展实验二] 测定石头纸中碳酸钙的质量分数
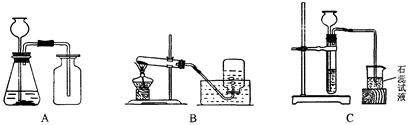
(2)甲组同学的方法是:(同温同压下,不同气体混合后体积等于混合前各气体体积之和。)将样品与稀盐酸反应,测定反应后生成CO2的体积,再换算为质量,最后根据CO2的质量求出样品中碳酸钙的质量。下图(Ⅰ)为石头纸与稀盐酸反应的装置,图(Ⅱ)用于测量CO2的体积。接仪器,夹紧弹簧夹,向a中加入一定量的水,如果a、b中有稳定的高度差,说明:装置(I)气密性 (选填“良好”或“漏气”)
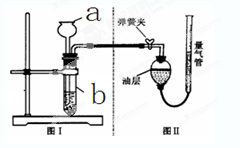
② 图(Ⅱ)装置中油层的作用是_ ;
③ 反应停止后, (填序号)可使反应前后
油层上方气体压强和外界大气压相同,此时
排出水的体积即为生成二氧化碳的体积。
A.水平移动量气管
B.上下移动量气管
[拓展实验一] 探究影响石头纸与盐酸反应快慢的因素
(1)甲、乙两同学设计实验如下:
| | 甲 | 乙 |
| 实验过程 | 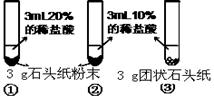 |  |
| 现象 | 试管①、②、③中产生气泡快慢的顺序为: ①>②>③。 |  |
| 分析结论 | Ⅰ 碳酸钙与稀盐酸反应的化学方程式为 Ⅱ 对比甲同学实验①②可知, ,化学反应的速度越快; Ⅲ 对比甲同学实验 (填实验序号)可知,反应物的接触面积越大,反应速率越 。 Ⅳ乙同学的实验中,数据记录纸上应该连续记录的实验数据是 和 。 | |
(2)甲组同学的方法是:(同温同压下,不同气体混合后体积等于混合前各气体体积之和。)将样品与稀盐酸反应,测定反应后生成CO2的体积,再换算为质量,最后根据CO2的质量求出样品中碳酸钙的质量。下图(Ⅰ)为石头纸与稀盐酸反应的装置,图(Ⅱ)用于测量CO2的体积。接仪器,夹紧弹簧夹,向a中加入一定量的水,如果a、b中有稳定的高度差,说明:装置(I)气密性 (选填“良好”或“漏气”)

② 图(Ⅱ)装置中油层的作用是_ ;
③ 反应停止后, (填序号)可使反应前后
油层上方气体压强和外界大气压相同,此时
排出水的体积即为生成二氧化碳的体积。
A.水平移动量气管
B.上下移动量气管
(1)ⅠCaCO3+2HCl=CaCl2+H2O+CO2↑;Ⅱ 盐酸的浓度越大(溶质质量分数越大) Ⅲ ②③;快 Ⅳ 时间;(计算器示数),锥形瓶及药品的质量(电子天平示数)或CO2的质量。
(2)①良好 ②防止CO2溶于水、与水反应或隔绝CO2与水 ③ B
(2)①良好 ②防止CO2溶于水、与水反应或隔绝CO2与水 ③ B
试题分析: (1)分析结论Ⅰ 碳酸钙与稀盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑Ⅱ 对比甲同学实验①②的不同知道二者的浓度不同,可知,盐酸的浓度越大,化学反应的速度越快;对比反应要控制变量只有一个条件不同才有对比性,Ⅲ 对比甲同学实验②③可知,反应物的接触面积越大,反应速率越快;Ⅳ由题中所给仪器可知,乙同学的实验中,数据记录纸上应该连续记录的实验数据是时间和锥形瓶及药品的质量;(2)①接仪器,夹紧弹簧夹,向a中加入一定量的水,试管内的液体被密封,如果a、b中有稳定的高度差,说明:气体的内外压不变,证明了装置(I)气密性良好;因为二氧化碳溶于水,所以② 图(Ⅱ)装置中油层的作用是防止CO2溶于水与水反应;③ 反应停止后,上下移动量气管可使反应前后
油层上方气体压强和外界大气压相同,此时排出水的体积即为生成二氧化碳的体积。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目