题目内容
把12克含杂质的石灰石(杂质不与酸反应)放在100g足量的稀盐酸里充分反应,反应停止后,所得混合物的总质量为107.6克,求:
(1)反应后生成的二氧化碳质量是多少?
(2)石灰石中碳酸钙的质量为多少?
解:(1)根据质量守恒定律可知质量的减少量是生成的二氧化碳的质量,所以生成二氧化碳的质量为:12g+100g-107.6g=4.4g;
(2)设要生成4.4g二氧化碳需要参加反应的碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
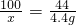
x=10g
答:(1)反应后生成的二氧化碳质量是4.4g;
(2)石灰石中碳酸钙的质量为10g;
分析:(1)依据质量守恒定律根据质量的减少量是生成的二氧化碳的质量即可;
(2)根据二氧化碳的质量利用有关的化学方程式计算出碳酸钙的质量;
点评:本题主要考查了质量守恒定律的应用和根据化学方程式进行有关的计算,要注意解题的步骤和计算结果的准确性,此题难度不大.
(2)设要生成4.4g二氧化碳需要参加反应的碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
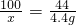
x=10g
答:(1)反应后生成的二氧化碳质量是4.4g;
(2)石灰石中碳酸钙的质量为10g;
分析:(1)依据质量守恒定律根据质量的减少量是生成的二氧化碳的质量即可;
(2)根据二氧化碳的质量利用有关的化学方程式计算出碳酸钙的质量;
点评:本题主要考查了质量守恒定律的应用和根据化学方程式进行有关的计算,要注意解题的步骤和计算结果的准确性,此题难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
 小明同学将12.5g含杂质的石灰石样品与100g足量的稀盐酸相混合(石灰石中的杂质不参加反应),充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示
小明同学将12.5g含杂质的石灰石样品与100g足量的稀盐酸相混合(石灰石中的杂质不参加反应),充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示