题目内容
【题目】工业上用闪锌矿(主要成分是ZnS,含有PbS等杂质)制备锌的流程如图(部分产物略去)
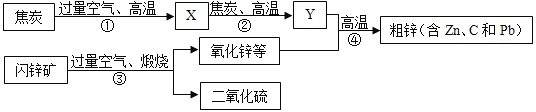
(1)焙烧时,产生的“气体M”为一种质量比为1:1的氧化物,其化学式为_____;
(2)流程中用过量空气的目的是_____;
(3)写出反应④中有ZnO参与的化学反应方程式_____;
(4)焦炭在上述流程中起着举足轻重的作用,下列属于焦炭作用的是_____;
a.作为燃料,为制备锌的化学反应提供能量
b.作为还原剂与二氧化碳反应
c.除去矿石中的杂质
物质 | Zn | Pb | C |
沸点℃ | 907 | 1749 | 4827 |
(5)根据上表数据:从粗锌中分离出纯锌的合适温度(t)的范围为_____。
【答案】SO2 使焦炭完全反应 ZnO+CO![]() Zn+CO2 ab 907℃<t<1749℃
Zn+CO2 ab 907℃<t<1749℃
【解析】
(1)二氧化硫中,硫元素与氧元素的质量比为32:(16×2)=1:1,所以气体氧化物M是二氧化硫;故填:SO2;
(2)焦炭在氧气充足时燃烧生成二氧化碳,用过量空气是为了保证让碳完全反应,故填:使焦炭完全反应;
(3)焦炭充分燃烧生成二氧化碳,在高温的条件下,二氧化碳与碳反应生成一氧化碳,所以X是二氧化碳,Y是一氧化碳,在高温的条件下,一氧化碳与氧化锌反应生成锌和二氧化碳;故填:ZnO+CO![]() Zn+CO2;
Zn+CO2;
(4)反应①是碳和氧气点燃生成二氧化碳,作为燃料提供热量,反应②是碳和二氧化碳高温反应生成一氧化碳,体现了碳具有还原性;故填:ab;
(5)根据表格提供的数据可以看出,锌的沸点比铅低,故可以将粗锌放在一容器中,保持温度907-1749℃,收集的锌蒸气,冷却后可得纯净的锌,故填:将粗锌放在一容器中,保持温度907-1749;收集的锌蒸气,冷却后可得纯净的锌;故填:907℃<t<1749℃。

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目