题目内容
【题目】实验室有一瓶硫酸溶液,老师请小明同学设计方案测定该溶液的溶质的质量分数。小明先取一只洁净的小烧杯,称其质量为16.4g,然后往其中倒入少量硫酸溶液后称量,总质量为30.2g,之后,将一枚质量为11.8g的铁钉(已用砂纸打磨去除铁锈)放入该小烧杯中,待铁钉表面不再有气泡产生后,再次称量,总质量为41.9g。请回答下列问题:
(1)写出上述反应的化学方程式是 。
(2)反应后产生的气体的质量是 。
(3)计算该硫酸溶液的溶质的质量分数(写出计算过程,计算结果精确到0.1%)。
【答案】
(1)Fe+H2SO4═FeSO4+H2↑ (2)0.1g (3)35.5%
【解析】
试题分析:
(1)铁和稀硫酸反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑。故填:Fe+H2SO4═FeSO4+H2↑。
(2)反应产生氢气的质量为:30.2g+11.8g﹣41.9g=0.1g,故填:0.1g。
(3)设硫酸的质量为x,
Fe+H2SO4═FeSO4+H2↑,
98 2
x 0.1g
![]()
x=4.9g
该废液中硫酸的溶质质量分数为:![]() ×100%≈35.5%。
×100%≈35.5%。
答:该硫酸溶液的溶质的质量分数为35.5%。

【题目】今年世界环境日中国的主题是:“改善环境质量,推动绿色发展”
①我们需要清新的空气。口罩中填充活性炭是利用其 性,以减少污染物的吸入。
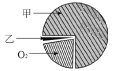
空气的组成(按体积分数)见下图,甲气体的名称是 ;乙中含多种气体,其中可用于填充飞艇且性质稳定的气体名称是 。
②我们需要结净的水源,含有杂质的天然水通过蒸发、沙滤、氧化等得到净化,其中氧化属于 变化)选填“物理”或“化学”),自来水生产通入氯气的作用是
③我们需要清洁、高效的能源,一氧化碳、氢气、甲烷中,最清洁的燃料是 .1mol燃料完全燃烧放出的热量见表.
燃料 | 一氧化碳 | 氢气 | 甲烷 |
热量(kJ) | 282.6 | 285.8 | 890.3 |
等物质的量的上述完全燃烧,放出热量最多的是 .甲烷(CH4)是天然气的主要成分,1molCH4约含有 个碳原子(用科学记数法表示).
【题目】兰兰在家里发现了一包过期的海苔,包装内有一个小纸袋,上面写着“石灰干燥剂”(主要成分为CaO),海苔过期了,石灰干燥剂有没有变质呢?兰兰拿着这包石灰干燥剂约化学老师一起到实验时进行如下探究.
【辨析俗称】“石灰干燥剂”中的石灰是指__________(填字母)
A.消石灰 B.生石灰 C.石灰石
【猜想与假设】猜想一:石灰干燥剂没有变质; 猜想二:石灰干燥剂部分变质;
猜想三:石灰干燥剂完全变质.
【进行实验】兰兰分别取该石灰干燥剂进行如表实验,并记录.
实验目的 | 实验步骤 | 实验现象 | 实验结论 |
实验一:验证有无CaCO3 |
| __________ | 猜想一不成立 |
实验二:__________ |
| 无明显放热现象 | 猜想三成立 |
【异常现象】兰兰整理实验,清洗仪器时,突然发现实验二中的烧杯壁明显发热.
【分析释疑】实验二的结论不准确,请用化学方程式解释烧杯壁明显发热的原因:__________.
【更正结论】该石灰干燥剂部分变质,猜想二成立.
【反思与评价】石灰干燥剂表面的覆盖物,影响了正确结论的得出,兰兰由此联想到生活中有些物质表面的覆盖物,是起保护作用的,试举一例:__________.
【拓展延伸】从确定这包石灰干燥剂成分的角度,请你再提出一个具有探究价值的问题:__________。