题目内容
【题目】粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。某班同学在粗盐提纯实验中,为把少量可溶性杂质CaCl2,MgCl2一并除去,将教材中实验方案修改设计如下,请据此回答问题:
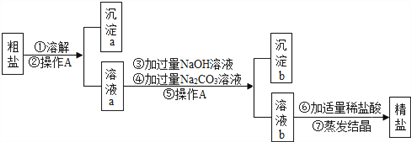
⑴实验操作A的名称是_________,该操作的目的是________________________。
⑵写出步骤③中发生反应的主要化学方程式____________________________;步骤⑥的作用是_______________________________;
⑶步骤⑦蒸发时玻璃棒的作用________________________________________________。
⑷小刚同学认为该方案实际得到的氯化钠可能比粗盐中含有的氯化钠要多,请你为他找出理由:_______________________________________________
【答案】 过滤 除去难溶性杂质 MgCl2+2NaOH═Mg(OH)2↓+2NaCl 除去过量的氢氧化钠和碳酸钠 搅拌,防止液体局部温度过高造成液滴飞溅 因为在实验过程中有氯化钠生成
【解析】粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。⑴实验操作A的名称是过滤,过滤是把不溶于液体的固体物质跟液体分离的一种方法。该操作的目的是除去难溶性杂质。⑵步骤③中发生反应的主要化学方程式是. MgCl2+2NaOH═Mg(OH)2↓+2NaCl;步骤⑥的作用是. 除去过量的氢氧化钠和碳酸钠,盐酸与氢氧化钠反应生成氯化钠和水,与碳酸钠溶液反应生成氯化钠,水和二氧化碳。⑶步骤⑦蒸发时玻璃棒的作用是搅拌,防止液体局部温度过高造成液滴飞溅。⑷该方案实际得到的氯化钠可能比粗盐中含有的氯化钠要多,理由:因为在实验过程中有氯化钠生成,盐酸与氢氧化钠和碳酸钠均生成了氯化钠。
点睛∶除杂原则⑴杂质尽量除净,⑵在除去一种杂质的同时不应增添新的杂质,⑶在除去杂质的同时,非杂物质不应过多消耗,但质量可以增加。

【题目】下图是用氯化钠溶液和氯化钾溶液制取氯酸钾的工艺流程,请根据题意回答下列问题。
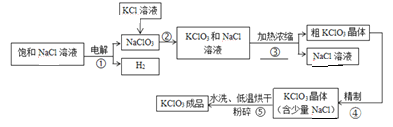
【资料】氯酸钾和氯化钠部分温度下的溶解度如下:
10℃ | 20℃ | 30℃ | 40℃ | |
氯酸钾 | 5.0g | 7.4g | 10.0g | 14.0g |
氯化钠 | 35.8g | 36.0g | 36.3g | 36.6g |
(1)请写出步骤②的化学方程式_________,该反应的基本反应类型是_________________。
(2)步骤③的操作分别是_________、过滤(填操作名称)。
(3)步骤⑤中是采用20℃以下的水进行洗涤,目的是①除去少量氯化钠②_____________。
(4)步骤⑤采用低温烘干,为什么不采用高温烘干___________________________(用化学方程式表示)。
【题目】学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200 g,平均分成4份进行实验,结果如下:
实验 | 一 | 二 | 三 | 四 |
加入样品的质量/g | 5 | 10 | 15 | 20 |
生成的CO2质量/g | 1.76 | 3.52 | 4.4 | m |
(1)上表中m的数值是 ;
(2)反应中矿石有剩余是第 次实验;
(3)这种石灰石矿中碳酸钙的质量分数是 ;
(4)稀盐酸中溶质的质量分数是 .