题目内容
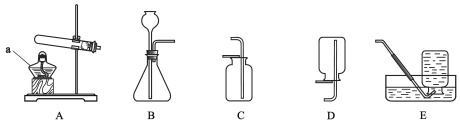
【题目】据新闻报道,每年因燃气热水器中毒意外身亡的事故不在少数,由于天燃气燃烧不充分,从而产生煤气中毒事故。某中学兴趣小组对煤气的成分产生了兴趣,化学老师提示他们,此煤气的成分可能是CO2、CO和H2O中的一种或几种。于是他们设计了如下实验来进行探究:
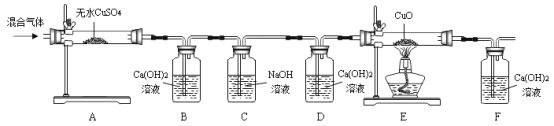
(1)A装置的作用是:_____;
(2)在实验前,应先通一段时间的混合气体再加热,目的是:_____;
(3)D装置在实验中所起的作用是:_____;
(4)在实验的过程中,观察到D中的澄清石灰水无变化,E中黑色粉末变成红色,B、F中变浑浊的现象后,大家一致得出结论,该煤气的组成为_____;
(5)小刚却指出,该实验中存在不足,请你指出不足之处:①_____;②_____。
【答案】检验混合气体中是否含有水 排尽玻璃管内空气,防止加热时发生爆炸 检验混合气体中的二氧化碳是否除尽 CO2和CO 没有尾气处理装置 装置最后没有吸收空气中二氧化碳的装置
【解析】
(1)无水硫酸铜与水会变蓝,A装置的作用是检验混合气体中是否含有水,故填:检验混合气体中是否含有水;
(2)实验开始时要先通一段时间混合气体再加热,目的是排尽玻璃管内空气,防止加热时发生爆炸;故填:排尽玻璃管内空气,防止加热时发生爆炸;
(3)D装置在实验中所起的作用是检验混合气体中的二氧化碳是否除尽;故填:检验混合气体中的二氧化碳是否除尽;
(4)氧化铜能与一氧化碳反应生成铜和二氧化碳,生成的二氧化碳能使F中的澄清石灰水变浑浊,在实验的过程中,观察到D中的澄清石灰水无变化,E中黑色粉末变成红色,B、F中变浑浊的现象后,该煤气的组成为CO2和CO;故填:CO2和CO;
(5)该实验的不足之处有:没有尾气处理装置,多余的一氧化碳会污染空气;装置最后没有吸收空气中二氧化碳的装置,F中澄清石灰水变浑浊可能是空气中的二氧化碳导致的。故填:没有尾气处理装置;装置最后没有吸收空气中二氧化碳的装置。

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案【题目】我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn) ,它可用来制造电器零件及日用品。将30g稀盐酸分三次加入到10g 黄铜样品粉末中(不考虑黄铜中的其他杂质),每次充分反应后,测定本次生成氢气的质量,实验数据见下表:
次数 | 第一次 | 第二次 | 第三次 |
加入稀盐酸的质量(g) | 10 | 10 | 10 |
本次生成氢气的质量(g) | 0.04 | m | 0.02 |
请回答:
(1)工业上常用铜作电缆的内芯,是利用铜具有良好的____________性。
(2) m=____________。
(3)所用稀盐酸的溶质质量分数___________? (结果精确到0.1)