题目内容
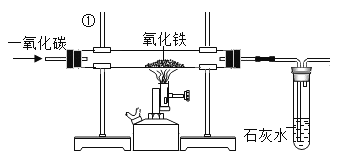
【题目】我国古代将炉甘石(ZnCO3)、赤铜(Cu20)和木炭粉混合后加热到一定温度,可以得 到一种外观似金子的锌和铜的合金,不法分子用它来冒充黄金,小晨同学在实验室进行了木炭粉王源氧化亚铜的实验(主要反应:C+Cu2O![]() 2Cu+CO↑),她观察到反应后的固体不完全是紫红色,于是对该固体的成分进行了实验探究:
2Cu+CO↑),她观察到反应后的固体不完全是紫红色,于是对该固体的成分进行了实验探究:
(提出问题)该固体的成分是什么?
(査阅资料)①Cu是紫红色固体
②Cu20是红色固体
③Cu20+H2SO4(稀)=CuSO4+Cu+H20
(猜想与假设)
猜想一:Cu;
猜想二 Cu、Cu20;
猜想三:Cu、C;
猜想四:Cu、Cu20、C
小晨同学认为猜想____________不正确,因为反应后的固体不完全是紫红色。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
取少量固体置于烧杯中,加入足量稀硫酸,观察溶液颜色 | 溶液呈①_____色 | 猜想三不正确 |
步骤二:把步骤一中所得混合物过滤,将滤渣干燥后置于滤纸上,观察固体颜色 | 固体为紫红色、黑色 | 猜想②_____正确 |
(实验反思)由于受反应物质量比、反应物接触面积和反应温度等因素的影响,固体物质性的反应可能无法完全进行。
(拓展延伸)
(1)从理论上看,碳与氧化亚铜的质量比应为1:12,但实际做实验时却将炭与氧化亚铜的质量比控制在约1:10。这样操作的理由是_______________。
(2)假黄金与硝酸银溶液反应的方程式是_________________________(写一个)。
【答案】一 蓝色 四 使氧化亚铜完全反应 Cu+2AgNO3=Cu(NO3)2+2Ag
【解析】
[猜想与假设]
铜是紫红色金属,观察到反应后的固体不完全是紫红色,所以猜想一不正确,故填一;
[实验探究]
①氧化铜和硫酸反应生成蓝色的硫酸铜和水,碳是黑色固体,若猜想三不正确,固体中应有氧化亚铜,加酸观察到溶液呈蓝色,故填蓝色;
②把步骤一中所得混合物过滤,将滤渣干燥后置于滤纸上,观察固体颜色为紫红色、黑色,说明猜想四正确,故填四;
[拓展延伸]
(1)从理论上看,碳与氧化亚铜的质量比应为1:12,但实际做实验时却将炭与氧化亚铜的质量比控制在约1:10,这样操作的理由是用足量的碳是氧化亚铜完全反应,故填使氧化亚铜完全反应;
(2)假黄金中的铜和锌都能和硝酸银反应,铜和硝酸银反应生成银和硝酸铜,方程式为Cu+2AgNO3=Cu(NO3)2+2Ag,锌和硝酸银反应生成硝酸锌和银,方程式为Zn+2AgNO3=Zn(NO3)2+2Ag,故填Cu+2AgNO3=Cu(NO3)2+2Ag(任写一个)。

【题目】下列实验现象及结论描述都正确的是( )
A | B | C | D | |
实验 |
|
|
|
|
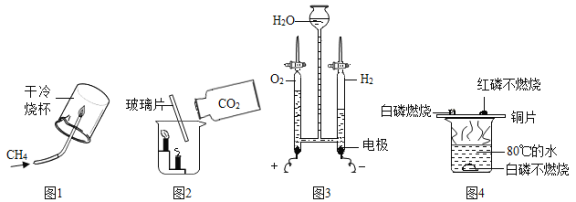
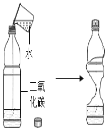
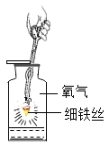
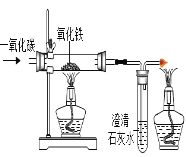
现象 | 旋紧瓶盖振荡, 塑料瓶变瘪 | 点燃的铁丝在氧气中 剧烈燃烧,火星四射, 生成四氧化三铁 | 加热后,氧化铜粉末变 红,澄清石灰水变浑浊 | 点燃某气体后、干冷烧杯内壁,出现无色液滴,澄清石灰水变浑浊 |
结论 | C02能溶于水 | 某些在空中不能燃烧的物质都可以在氧 中燃烧 | 一氧化碳能使氧化铜还原成铜,具有还原性 | 该气休屮一定饤碳元素、 从元系和元茗 |
A. A B. B C. C D. D