题目内容
【题目】下列实验能到实验目的是
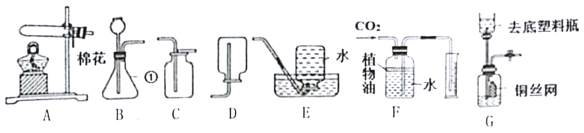
A.  探究铁锈蚀条件 B.
探究铁锈蚀条件 B.  探究燃烧条件
探究燃烧条件
C. 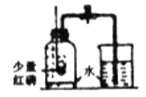 测定空气中氧气含量 D.
测定空气中氧气含量 D.  探究分子运动
探究分子运动
【答案】D
【解析】
A、铁锈蚀同时需要氧气和水,铁在干燥的空气中、在蒸馏水中均不生锈,不能探究铁锈蚀的条件,故不符合题意;
B、燃烧的三个条件为可燃物、和氧气接触、达到着火点,三者缺一不可,图中无法得出燃烧必须与氧气接触的条件,不能达到目的,故不符合题意;
C、测定空气中氧气的含量,应将装置内的氧气完全消耗掉,应使用过量的红磷,图中红磷是少量的,不能达到目的,故不符合题意;
D、大烧杯装置外是一个对比实验,能证明氨水能使酚酞试液变红;由于浓氨水易挥发,大烧杯内的小烧杯内的酚酞试液逐渐变为红色,说明氨气分子不断运动扩散到了大烧杯内的酚酞小烧杯中,可以达到实验目的,故符合题意。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
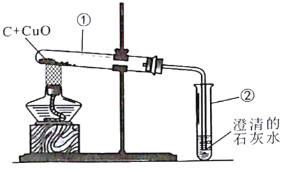
名师点睛字词句段篇系列答案【题目】我国古代将炉甘石(ZnCO3)、赤铜(Cu20)和木炭粉混合后加热到一定温度,可以得 到一种外观似金子的锌和铜的合金,不法分子用它来冒充黄金,小晨同学在实验室进行了木炭粉王源氧化亚铜的实验(主要反应:C+Cu2O![]() 2Cu+CO↑),她观察到反应后的固体不完全是紫红色,于是对该固体的成分进行了实验探究:
2Cu+CO↑),她观察到反应后的固体不完全是紫红色,于是对该固体的成分进行了实验探究:
(提出问题)该固体的成分是什么?
(査阅资料)①Cu是紫红色固体
②Cu20是红色固体
③Cu20+H2SO4(稀)=CuSO4+Cu+H20
(猜想与假设)
猜想一:Cu;
猜想二 Cu、Cu20;
猜想三:Cu、C;
猜想四:Cu、Cu20、C
小晨同学认为猜想____________不正确,因为反应后的固体不完全是紫红色。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
取少量固体置于烧杯中,加入足量稀硫酸,观察溶液颜色 | 溶液呈①_____色 | 猜想三不正确 |
步骤二:把步骤一中所得混合物过滤,将滤渣干燥后置于滤纸上,观察固体颜色 | 固体为紫红色、黑色 | 猜想②_____正确 |
(实验反思)由于受反应物质量比、反应物接触面积和反应温度等因素的影响,固体物质性的反应可能无法完全进行。
(拓展延伸)
(1)从理论上看,碳与氧化亚铜的质量比应为1:12,但实际做实验时却将炭与氧化亚铜的质量比控制在约1:10。这样操作的理由是_______________。
(2)假黄金与硝酸银溶液反应的方程式是_________________________(写一个)。