题目内容
【题目】某化学活动小组在一次实验中进行了如图所示实验:
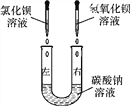
此时观察到的实验现象是______________________________________________。
实验后,小组同学充分振荡U形玻璃管,将U形玻璃管内的物质过滤后,对滤液成分产生了浓厚的兴趣,进行了进一步的探究活动。
【提出问题】滤液中除Na+外,还含有什么离子?
【猜想与假设】A同学:含有OH-、Cl-、CO![]() 。
。
B同学:含有OH-、Cl-、Ba2+。
C同学:含有____________(填离子符号)。
【实验探究】B同学为了验证自己的猜想,取少量滤液于试管中,向其中滴加少量的硫酸钠溶液,观察到无明显现象。由此B同学得出结论:自己的猜想不成立,A同学的猜想成立。
【评价与交流】请你评价B同学的结论:________________________________。同学们经过讨论后一致认为:B同学在验证自己的猜想时,若将所加试剂调换成足量的另一种试剂________(填化学式),既能验证自己的猜想,也能确定滤液中的离子成分。
C同学取该试剂进行实验,最终确定了滤液中的离子成分。
【归纳与总结】通过上述实验我们能够总结出:在确定化学反应后所得溶液中的离子成分时,一般应加入____________________,验证____________________就可以确定溶液中的离子成分。
【答案】 U形玻璃管左、右两端均产生白色沉淀 OH-、Cl- B同学的结论不完全正确(或B同学的结论不正确) H2SO4 适当的、适量的试剂 (溶液中)可能存在的离子是否存在
【解析】 (1). 碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,和氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,所以现象是U形玻璃管左、右两端均产生白色沉淀; (2). 反应后溶液中一定有氢氧化钠和氯化钠,离子除钠离子外一定有OH-、Cl-,当刚好完全反应时只有钠离子、氯离子和氢氧根离子; (3). 取少量滤液于试管中,向其中滴加少量的硫酸钠溶液,观察到无明显现象,只能说明没有钡离子,B同学的猜想不成立;溶液中还有的离子可能是OH-、Cl-、CO![]() ,也可能是OH-、Cl-,即A同学的猜想不一定成立; (4). 若将所加试剂调换成足量的 H2SO4,通过观察是否有气泡产生,就能确定是否有碳酸根离子了,也就能证明A和C谁的猜想成立了; (5). 通过上述实验我们能够总结出:在确定化学反应后所得溶液中的离子成分时,一般应加入适当的、适量的试剂,验证(溶液中)可能存在的离子是否存在就可以确定溶液中的离子成分。
,也可能是OH-、Cl-,即A同学的猜想不一定成立; (4). 若将所加试剂调换成足量的 H2SO4,通过观察是否有气泡产生,就能确定是否有碳酸根离子了,也就能证明A和C谁的猜想成立了; (5). 通过上述实验我们能够总结出:在确定化学反应后所得溶液中的离子成分时,一般应加入适当的、适量的试剂,验证(溶液中)可能存在的离子是否存在就可以确定溶液中的离子成分。