题目内容
【题目】请根据如图所示的内容填空。
A B
B C
C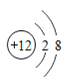 D
D E
E
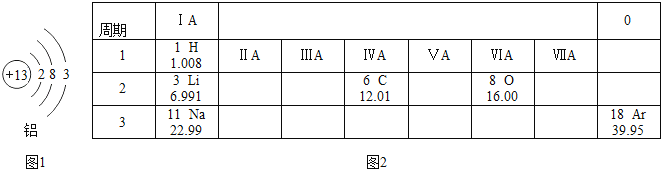
①图E结构最外层电子数是_____,在化学反应中容易_____(填“得”或“失”)电子,形成离子符号为_____,它与氯元素形成化合物的化学式为_____。
②A.B.C.D.E中,对应单质化学性质最稳定的是_____(填序号,下同),属于同一种元素的是_____和_____。
【答案】2 失 Mg2+ MgCl2 B C E
【解析】
由图可知A是氟原子,B是氖原子,C是镁离子,D是钠原子,E是镁原子。
①由原子结构示意图可知,微粒E的质子数是12,微粒A最外层电子数是2,小于4,在化学反应中容易失电子;形成离子符号为:Mg2+;它与氯元素形成化合物的化学式为:MgCl2。
②微粒A.B.C.D.E中,B的原子的最外层电子数是8,达到了稳定结构,对应单质化学性质最稳定,质子数决定元素的种类,CE中质子数相同,属于同一种元素。

【题目】化学兴趣小组做酸和碱的中和反应时,往NaOH溶液中滴入几滴酚酞溶液,发现溶液刚变
红瞬间又褪成无色。讨论并猜想。
猜想一:可能是酚酞溶液变质
猜想二:可能与NaOH溶液的浓度有关
猜想三:可能是酚酞溶液在滴入过程中被O2氧化
……
(1)甲同学认为猜想一是不对的。其理由是_________________________。
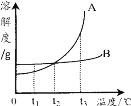
(2)取3mL不同浓度的NaOH溶液,分别滴入3滴酚酞溶液,观察现象。得到NaOH溶液的浓度与酚酞溶液褪色时间关系如图2所示。
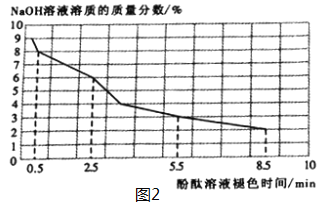
①根据图2所示,NaOH溶液溶质的质量分数________,酚酞溶液由红色褪为无色的时间越短。
②做酸和碱的中和反应时,滴加酚酞溶液的目的是________________________________。若用做实验的NaOH溶液溶质的质量分数为4%,完成该实验的操作时间应控制在_______之内。
(3)请设计实验,验证猜想三是否正确。
实验操作 | 实验现象 | 实验结论 |
__________ | 5.5min酚酞溶液褪色 | 酚酞溶液先变红后褪色与O2_______ (选填“有关”或“无关”) |
(4)探究酸碱中和反应时,逐滴加入稀盐酸的过程,并不断搅拌的目是_________________,写出该反应的化学方程式___________________________。
【题目】某兴趣小组同学对实验室制备氧气的条件进行探究实验。
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计对比实验:
Ⅰ.将3.0g氯酸钾与1.0g二氧化锰均匀混合加热;
Ⅱ.将xg氯酸钾与1.0g氧化铜均匀混合加热。
在相同温度下,比较两组实验产生氧气的快慢。
Ⅰ中反应的符号表达式是_____,Ⅱ中x的值应为_____
(2)乙探究了影响双氧水分解速度的某种因素。实验数据记录如下:
双氧水的质量(g) | 双氧水的浓度 | 二氧化锰的质量(g) | 相同时间内产生氧气的体积(mL) | |
Ⅰ | 50.0 | 1% | 0.1 | 9 |
Ⅱ | 50.0 | 2% | 0.1 | 16 |
Ⅲ | 50.0 | 4% | 31 |
①取用二氧化锰的仪器是_____,实验Ⅲ中,加入二氧化锰的质量为_____g。
②实验结论:在相同条件下,_____,双氧水分解得越快。