题目内容
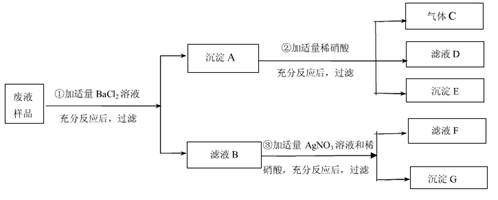
(6分)某食盐样品中含有少量沙土、氯化钙和氯化镁.以下是除去食盐样品中沙土、氯化钙和氯化镁的实验流程: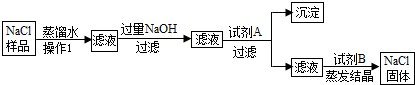
根据流程图回答:
(1)操作Ⅰ的名称是 ,加入的试剂A是 ,沉淀是
;
(2)写出NaOH与杂质反应的化学方程式 ;
(3)加入试剂B的目的是 ;
(4)蒸发结晶时用到玻璃棒的作用是 。
(1)过滤 Na2CO3 =CaCO3
(2)2NaOH + MgCl2 = Mg(OH)2↓ + 2NaCl
(3)除去NaOH和Na2CO3
(4)防止局部温度过高,造成液滴飞溅
解析试题分析:(1)操作Ⅰ是将不溶性固体也液体分离,所以名称为:过滤,在滤液中加入过量的NaOH溶液是除去杂质氯化镁,故接下来加入的试剂A,是为了除去氯化钙,所以加入的试剂A应是Na2CO3溶液,发生反应:CaCl2+Na2CO3==CaCO3↓+2NaCl,所以沉淀是:=CaCO3
(2)根据上面的分析,NaOH与杂质反应的化学方程式:2NaOH + MgCl2 = Mg(OH)2↓ + 2NaCl
(3)由于前面所加试剂都是过量,所以试剂B是将前面所加过量的NaOH和Na2CO3除去
(4)蒸发结晶时用到玻璃棒的作用是:防止局部温度过高,造成液滴飞溅
考点:物质的除杂

碳酸氢钠常用于食品和医药工业,某化学兴趣小组对碳酸氢钠进行探究。
【查阅资料】 Ⅰ.碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质。
Ⅱ.碳酸钠溶液呈碱性。
【进行实验】为了验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠到铜片上加热,如图所示。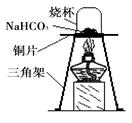
(1)加热一段时间后,观察到烧杯内壁有__________。
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊。写出该反应的化学方程式:___________________。
(3)兴趣小组的同学认为:充分加热后的固体产物可能是NaOH或Na2CO3。
①他们的依据是____________________________________。
②兴趣小组为了确定反应后的固体产物成分进行以下实验,请填写下表:
| 实验 | 实验现象 | 结论 |
| 实验一:取少量反应后的固体产物溶于水,滴入几滴酚酞试液 | 溶液变成红色 | 固体产物是NaOH,而不是Na2CO3 |
| 实验二:取少量反应后的固体产物溶于水,加入氯化钙溶液 | _____________ | 固体产物是Na2CO3,而不是NaOH |
| 实验三:___________________ ___________________________ | 产生大量气泡 | 固体产物是Na2CO3,而不是NaOH |
【讨论与评价】实验一的结论与实验二、实验三的结论相反,在讨论时兴趣小组的同学认为方案一的结论不正确,他们的理由是_____________________________________________。
【总结】请写出碳酸氢钠受热分解的化学方程式________________________。
(4)某碱厂的主要产品之一是小苏打(碳酸氢钠),为了测定产品中碳酸氢钠的质量分数(假设该样品中只含氯化钠一种杂质),取样品10.0 g逐滴加入稀盐酸,所得气体的质量为4.4 g。求:样品中碳酸氢钠的质量分数。
下图为NaCl、KNO3的溶解度曲线,下列说法正确的是
| A.KNO3的溶解度一定大于NaCl溶解度 |
| B.20℃时,50g水最多能溶解31.6gKNO3 |
| C.t℃时,NaCl和KNO3的饱和溶液的溶质质量分数相等 |
| D.50℃的NaCl饱和溶液降温到20℃时变成不饱和溶液 |