题目内容
【题目】化学是一门以实验为基础的科学,请结合图示回答问题:
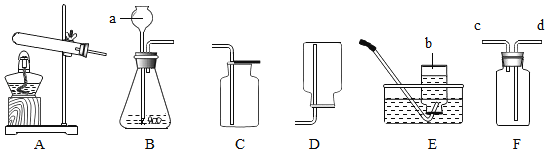
(1)实验室准备用高锰酸钾制取比较纯净的氧气,采用的装置组合是_____,该反应的化学方程式为_____;
(2)实验室用于制取二氧化碳的方程式为_____.
采用的常见装置组合为_____,酸液应从_____加入(写仪器名称);
若小华想用F装置收集一瓶该气体,则气体由_____(填c或d)端进入.
(3)实验室制取二氧化碳一般有以下步骤:
①检查装置的气密性;②按要求连接制取装置;③向长颈漏斗中注入盐酸;④收集气体;⑤向大试管内放入石灰石,操作顺序正确的是_____
A.①②③④⑤B.②①③④⑤C.②①⑤③④D.③④⑤②①
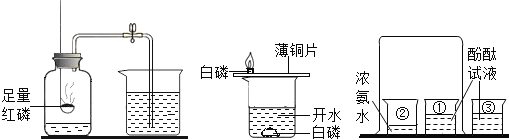
(4)该小组在制取CO2的时候,发现二氧化碳收集好后,反应仍在发生,所以,他们想设计一个能随时控制反应的发生与停止的装置.你觉得下图Ⅰ、Ⅱ、Ⅲ装置中能实现上述意图的是_____.

【答案】AE;2KMnO4![]() K2MnO4+MnO2+O2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ BC 长颈漏斗 d C ①和③
K2MnO4+MnO2+O2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ BC 长颈漏斗 d C ①和③
【解析】
根据高锰酸钾受热分解会生成锰酸钾、二氧化们和氧气书写化学反应方程式;根据化学实验基础及操作注意事项分析解答。
(1)氧气不易溶于水,密度比空气大,故可用排水法或向上排空气法收集,制取较纯净的氧气,可用排水法;根据反应物是固体,反应条件为加热,所以发生装置选择A;高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,方程式为2KMnO4![]() K2MnO4+MnO2+O2↑;故答案为:AE;2KMnO4
K2MnO4+MnO2+O2↑;故答案为:AE;2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(2)碳酸钙和盐酸常温下反应生成氯化钙、二氧化碳气体和水,方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,属于固液常温型,故选择装置B来制取,长颈漏斗是用来添加稀盐酸的;二氧化碳能溶于水,密度比空气大,所以用装置C来收集;二氧化碳比空气的密度大,用F装置收集二氧化碳,气体应从长进短出.故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;BC;长颈漏斗;d;
(3)制取二氧化碳首先是对装置的连接,接着检查装置的气密性,然后是加入药品,即先向反应容器中放入大理石,再向漏斗中注入稀盐酸,最后收集气体;故答案为:C;
(4)分析图中的装置可以知道,①中的隔板可以放置固体,当用止水夹夹住胶皮管时由于气体不能逸散而使试管中压强增大,将液体压到长颈漏斗中,此时固液分离而使实验停止,若使实验开始只要将止水夹打开即可;装置②中用的普通漏斗,难以实现固液分离,而装置③中破了的试管起到了装置中隔板的作用,具体使用时将试管放入试管中,若停止实验只要将试管取出即可.所以能够实现随时开始或终止实验的装置为:①和③.故答案为:①和③。

 优学名师名题系列答案
优学名师名题系列答案【题目】实验探究:
央视频道《是真的吗?》栏目中有一段视频:将“锡纸”剪成一段两头宽中间窄的纸条,然后两头分别连接电池的正负极,观察到“锡纸”立即燃烧。据此,某同学取“锡纸”进行了以下探究:
探究一:“锡纸”燃烧的原因
“锡纸”两端接入电池两极后造成短路致使“锡纸”燃烧,从燃烧的条件开始“锡纸”不燃烧但短路后却能燃烧的原因是______。
探究二:“锡纸”中金属的成分
(提出问题)“锡纸”中的金属是锡吗?
(査阅资料)①“锡纸”是锡箔或铝箔
②锌粉是一种深灰色固体
③锡(Sn)与酸或金属化合物溶液反应生成+2价锡的化合物
(提出猜想)猜想I:“锡纸”中的金属是锡猜想Ⅱ:“锡纸”中的金属是铝
(进行实验)设计方案并进行实验
实验操作 | 实验现象 | 实验分析与结论 |
取打磨后的“锡纸”片放入 试管中,滴加氯化锌溶液 | “锡纸”表面有 深灰色固体析出 | 根据实验现象,结合金属活动性顺序 可知猜想 ______ 成立;反应的化学方程式为 ______ 。 |
(交流讨论)(1)实验中打磨“锡纸”的目的是______。
(2)下列物质的溶液可以替代氯化锌溶液完成上述实验的是______(填字母序号)
A.氯化铜 B.硝酸银 C.硫酸钠 D.硫酸亚铁
(拓展应用)证明铁、铜、银三种金属活动性顺序的实验方案如下,请将内容补充完整
实验操作 | 实验现象 | 实验结论 |
| 若A/B为金属,则C为 ______ (填名称)溶液,则发生反应的试管中观察到的现象为 ______ , 反应的化学方程式为 ______ 。 | 铁、铜、银三种金属的活动性顺序是: Fe>Cu>Ag |