题目内容
4分)某化学小组同学欲测定铜锌合金中铜元素的质量分数。
(1)甲方案:取10g合金粉末,加入少量稀硫酸后,收集到0.1g氢气,计算合金中铜元素的质量分数为62.5%。老师指出其测定结果不准确,原因是 。
(2)乙方案:取10g合金粉末,加入足量硫酸铜溶液,充分反应后,过滤,洗涤,烘干,测得固体质量为9.9g。计算合金中铜元素的质量分数。
(1)甲方案:取10g合金粉末,加入少量稀硫酸后,收集到0.1g氢气,计算合金中铜元素的质量分数为62.5%。老师指出其测定结果不准确,原因是 。
(2)乙方案:取10g合金粉末,加入足量硫酸铜溶液,充分反应后,过滤,洗涤,烘干,测得固体质量为9.9g。计算合金中铜元素的质量分数。
(1)加入少量稀硫酸后,合金中的锌是否完全反应无法确定;(2)35%
试题分析:(1)因为加入的是少量的稀硫酸,不能保证合金中的锌完全反应,所以计算结果不准确;(2)解:设合金中锌的质量为x,
Zn+CuSO4═ZnSO4+Cu 反应前后固体的质量差
65 64 65-64=1,
x 10g-9.9g
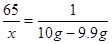 解得x=6.5g;合金中铜的质量分数为:
解得x=6.5g;合金中铜的质量分数为: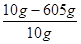 ×100%=×100%=35%;
×100%=×100%=35%;答:合金中铜的质量分数为35%.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目