题目内容
实验课上,老师安排了分组实验,甲组同学制取O2,乙组同学制取CO2.(1)实验室制取气体的发生装置和收集装置类型的确定应根据______(填序号)
a.化学药品的状态 b.发生化学反应的条件
c.生成气体的密度和在水中的溶解性
(2)甲组同学若用高锰酸钾制取氧气,反应方程式为______ K2MnO4+MnO2+O2↑,
【答案】分析:(1)根据发生装置和收集装置的选择依据即可.
(2)根据氧气的实验室制法即可.
(3)根据二氧化碳的实验室制法和反应装置即可.
(4)
[作出猜想]盐酸可能会剩余.
[实验与结论]
②根据酸和碱遇到指示剂的颜色变化即可.
③只要可以和盐酸反应,并且有明显现象即可.
[拓展与应用]
①根据除杂的条件即可.
②答案合理即可.
解答:解:
(1)常见的发生装置有三种,①固体和固体加热制气体,②固体和液体不加热,③固体和液体加热;收集装置常见的也有三种,①气体不溶于水,采用排水法,②密度比空气大,采用向上排空气法,③密度比空气小,采用向下排空气法;故答案为:a、b、c.
(2)这是氧气的实验室制法之一,故答案为:2KMnO4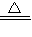 K2MnO4+MnO2+O2↑,催化,过滤;
K2MnO4+MnO2+O2↑,催化,过滤;
(3)这是二氧化碳的实验室制法,发生装置属于固体和液体不加热制取气体,收集装置属于向上排空气法收集;故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑,A、C、D.
(4)
[作出猜想]:实验室用石灰石和稀盐酸制取CO2,反应后,盐酸可能有剩余,故答案为:HCl.
[实验与结论]
②CaCl2是中性,HCl是酸性,中性物质和酸性物质都不能使酚酞颜色发生变化,故答案为:不能,酚酞遇酸也不变色③盐酸能够是石蕊试液变红,但是CaCl2不能使石蕊变红,所以可用石蕊.故答案为:石蕊,石蕊试液变红.(其它答案合理均可).
①CaCO3 和盐酸反应生成CaCl2和二氧化碳和水,剩余的碳酸钙过滤即可,故答案为:CaCO3.
②根据酸的性质可知,故答案为:腐蚀铁质水管,污染水源等.
点评:这个题涉及知识要点较多,掌握发生装置和收集装置的选择条件以及常见气体的实验室制法,掌握除杂的要求和指示剂的颜色变化规律.
(2)根据氧气的实验室制法即可.
(3)根据二氧化碳的实验室制法和反应装置即可.
(4)
[作出猜想]盐酸可能会剩余.
[实验与结论]
②根据酸和碱遇到指示剂的颜色变化即可.
③只要可以和盐酸反应,并且有明显现象即可.
[拓展与应用]
①根据除杂的条件即可.
②答案合理即可.
解答:解:
(1)常见的发生装置有三种,①固体和固体加热制气体,②固体和液体不加热,③固体和液体加热;收集装置常见的也有三种,①气体不溶于水,采用排水法,②密度比空气大,采用向上排空气法,③密度比空气小,采用向下排空气法;故答案为:a、b、c.
(2)这是氧气的实验室制法之一,故答案为:2KMnO4
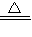 K2MnO4+MnO2+O2↑,催化,过滤;
K2MnO4+MnO2+O2↑,催化,过滤;(3)这是二氧化碳的实验室制法,发生装置属于固体和液体不加热制取气体,收集装置属于向上排空气法收集;故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑,A、C、D.
(4)
[作出猜想]:实验室用石灰石和稀盐酸制取CO2,反应后,盐酸可能有剩余,故答案为:HCl.
[实验与结论]
②CaCl2是中性,HCl是酸性,中性物质和酸性物质都不能使酚酞颜色发生变化,故答案为:不能,酚酞遇酸也不变色③盐酸能够是石蕊试液变红,但是CaCl2不能使石蕊变红,所以可用石蕊.故答案为:石蕊,石蕊试液变红.(其它答案合理均可).
①CaCO3 和盐酸反应生成CaCl2和二氧化碳和水,剩余的碳酸钙过滤即可,故答案为:CaCO3.
②根据酸的性质可知,故答案为:腐蚀铁质水管,污染水源等.
点评:这个题涉及知识要点较多,掌握发生装置和收集装置的选择条件以及常见气体的实验室制法,掌握除杂的要求和指示剂的颜色变化规律.

练习册系列答案
相关题目
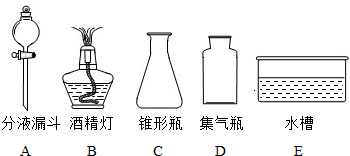
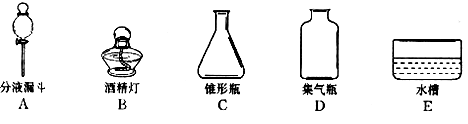
 (3)乙组同学制取CO2的反应化学方程式 ,其发生装置和收集装置的装配,应选用的仪器有:带导管的双孔塞、玻璃片以及下图所示中的 (填标号)等.
(3)乙组同学制取CO2的反应化学方程式 ,其发生装置和收集装置的装配,应选用的仪器有:带导管的双孔塞、玻璃片以及下图所示中的 (填标号)等.
 (3)乙组同学制取CO2的反应化学方程式 ,其发生装置和收集装置的装配,应选用的仪器有:带导管的双孔塞、玻璃片以及下图所示中的 (填标号)等.
(3)乙组同学制取CO2的反应化学方程式 ,其发生装置和收集装置的装配,应选用的仪器有:带导管的双孔塞、玻璃片以及下图所示中的 (填标号)等.