��Ŀ����
����Ŀ����������װ�ã��ش����⣺

(1)д��ͼ�б�����������ƣ���___________����___________��
(2)ʵ������п����ϡ���ᷴӦ��ȡ����ʱ��������Ӧ�Ļ�ѧ����ʽΪ_________________���ӿ��Ʒ�Ӧ���ʺͽ�ԼҩƷ�ĽǶȿ��ǣ�����װ�����ѡ��_____(��װ�����)��
(3)��Ϊ������������ˮ�����Կ�������װ��_______(��װ�����)�ռ������Ҫ����˿��������ȼ�յ�ʵ�飬������װ���ռ�����ʱӦע��_______________________��
(4)ʵ������ȡ������̼����װ�ÿ�ѡ��װ��A��װ��B��װ��C��װ��B��װ��A��C��ȣ�װ��B�ŵ���_______________��������̼���ռ�װ����_____(��װ����ĸ)��ʵ������ȡ������̼�Ļ�ѧ����ʽΪ____________________��
���𰸡� ��Һ©�� �Թ� Zn + H2SO4 =Zn SO4+ H 2�� B F �ڼ���ƿ��Ԥ������ˮ ��ʱ���Ʒ�Ӧ���� E CaCO3+2HCl=CaCl2+H2O+CO2��
����������1�������ٵ������Ƿ�Һ©���������ڵ��������Թܣ�
��2��п��ϡ���ᷴӦ��������п����������Ӧ����ʽΪZn + H2SO4 =Zn SO4+ H 2����Bװ���÷�Һ©������ϡ���ᣬ���Կ��Ʒ�Ӧ���ʺͽ�ԼҩƷ����ѡB��
��3��������������ˮ������ѡ����ˮ��װ��F�ռ�����˿��������ȼ�յ��������¶ȼ��ߣ�Ϊ�˷�ֹƿ��ը�ѣ����ռ�����ʱ���ڼ���ƿ��Ԥ������ˮ��
��4��װ��B����ϡ�������÷�Һ©�������ŵ��ǿ�����ʱ���Ʒ�Ӧ���ʣ�������̼������ˮ���ܶȱȿ������ܶȴ�ѡ�����ſ�����װ��E�ռ���ʵ�����ô���ʯ��ϡ���ᷴӦ���ɶ�����̼���Ȼ��ƺ�ˮ����ȡ������̼����Ӧ����ʽCaCO3+2HCl=CaCl2+H2O+CO2����

����Ŀ��ˮ��������Ϥ�����ʡ�
��Ϊ�˲ⶨˮ����ɣ���������̽����
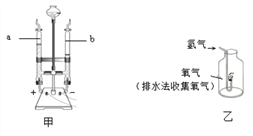
���������ˮʱ�������ڵ�������____________��b�������ɵ�������______________������a���ڲ�������ķ�����___________������������������___________����ʵ��˵��ˮ�����⡢��Ԫ����ɵ�����������__________��
���ˮʱ��������������������ʹ���ˮ��Ӧ�����У����������Ʊ����������ͻ�ѧ���ʲ������仯����ˮ���װ����ʢ��һ����������������Һ��ͨ��һ��ʱ�������16g������������Һ���������Ƶ����������� 2.7%��Ϊ3.0%���Լ���
��.�μӷ�Ӧ��ˮ�����ʵ���____________mol(���ݻ�ѧ����ʽ��ʽ����)��
��.���ǰ����������Һ������Ϊ________________g��
�ҷ������÷�����ʵ��Ŀ����____________________��������������ȼ�գ���Ӧ�Ļ�ѧ����ʽ��_________________������__________����ʵ���ܷ�ﵽʵ��Ŀ�ģ�����������___________��
���±���KNO3 ��NaCl�ڲ�ͬ�¶��µIJ����ܽ�����ݡ�
�¶�(��) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
KNO3 | 13.3 | 20.9 | 32.0 | 45.8 | 64.0 | 85.5 | 110.0 | 138.0 | 169.0 | 202.0 | 246.0 |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 | 39.0 | 39.8 |
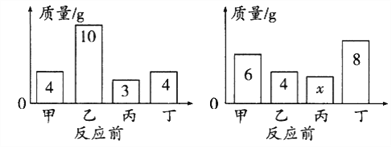
��. �������������ܽ�ȵı仯���¶�Ӱ���С����___________��
��. ��40��ʱ����40gKNO3�ܽ���50gˮ�У��γ���Һ��������_______g����������60�棬�γɵ���ҺΪ________(����������������������)��Һ������Һ��������������Ϊ_______��
��.���ݱ������ݣ��ҳ�60.0gˮ�ܹ��ܽ�66.0g KNO3���¶ȷ�Χ��___________��
��. ����KNO3�л�������NaCl�����ᴿKNO3�����ʵ�鲽��Ϊ________��
��.������ˮ�е��ܽ��Ҳ��һ���ı仯���ɡ���ͼΪ��ͬ�¶��£�ij������ܽ�����¶ȵĹ�ϵ��
ͼ��P1��P2��ʾ��ѹ����P1��P2�Ĺ�ϵ��________��
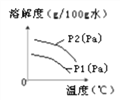
A.P1��P2
B.P1��P2
C.P1��P2
D.��ȷ��
����Ŀ����������װ�ûش����⣺
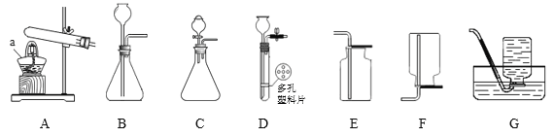
�� д������������ƣ�a ______________��
�� ���������װ��A��������,���Թܿ���ˮ����֣���������______��ѡ���������ѧ�����仯����ġ�
�� �÷�ĩ״̼�����ϡ���ᷴӦ�ƶ�����̼����ʹ��Ӧƽ�Ƚ��еķ���װ����_________��д���÷�Ӧ�Ļ�ѧ����ʽ_______________���ռ�������̼������������Eװ�õ�ԭ����_______________��
�� ̽������������Թ�������ֽ����ʵ�Ӱ�죬ʵ���������±���������Ӱ��ʵ������ؾ���ͬ��
��� | ����������Һ����/�� | ��������/�� | ��������/�� |
ʵ��1 | 100.0 | MnO2 0.2 | t1 |
ʵ��2 | 100.0 | CuO X | t2 |
��.����X����ֵӦ��______��
��.���еĴ�������ָ�����ռ���ͬ�����������ʱ�䣬��t1____��ѡ�>������<����=����t2����MnO2�Ĵ�Ч������CuO���������Բ���__________��Ҳ�ܴﵽʵ��Ŀ�ġ�
��.���ʵ��1����ȫ��Ӧ����������1.6�ˣ������������Һ����������������__________�������ݻ�ѧ����ʽ���㣩
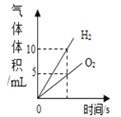
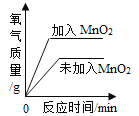
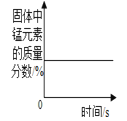
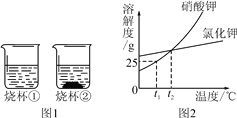
����Ŀ������4��ͼ���У�����ȷ��Ӧ�仯��ϵ����( )
|
|
|
|
A�����ˮ������������ | B�����ݵ����5%�Ĺ���������Һ��������һ�ݼ��������������� | C������һ�������ĸ�����ع��� | D���ں��������£������͵�KNO3��Һ��������ˮ |
A. A B. B C. C D. D