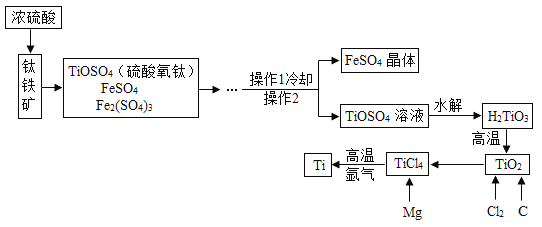
题目内容
【题目】现有一包含有杂质的BaCl2固体样品(杂质不溶于水),为了研究样品的组成,进行了如下试验。请回答下列问题:
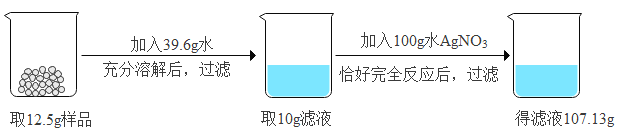
(1)实验发生反应的化学方程式为____________________________。
(2)列出求解10g滤液中溶质质量(x)的比例式_______________________。
(3)AgNO3溶液的溶质质量分数为_______________________。
(4)样品固体加水充分溶解后,所得溶液的溶质质量分数为_______________________。
(5)加入硝酸银溶液的过程中,用数据说明滤液中溶质的变化情况是________________。
(6)样品中BaCl2的含量为_______________________。
【答案】BaCl2+2AgNO3=2AgCl↓+Ba(NO3)2 ![]() 3.4% 20.8% 氯化钡的质量由2. 08g减少至0g,硝酸钡的质量由0g增加至2.61g 83. 2%
3.4% 20.8% 氯化钡的质量由2. 08g减少至0g,硝酸钡的质量由0g增加至2.61g 83. 2%
【解析】
(1)实验发生的反应是氯化钡与硝酸银反应生成硝酸钡和氯化银,反应的化学方程式为:BaCl2+2AgNO3=2AgCl↓+Ba(NO3)2;
(2)根据题意可知,10g滤液反应生成的氯化银沉淀的质量=10g+100g-107.13g=2.87g;
设:10g滤液中溶质质量为x,参加反应的硝酸银质量为y,生成硝酸钡质量为z。

![]() x=2.08 g
x=2.08 g
![]() y=3.40g;
y=3.40g;
![]() z=2.61g;
z=2.61g;
(3)AgNO3溶液的溶质质量分数=![]() ;
;
(4)固体溶于水后得到的溶液,其质量分数和取出的10g溶液的相同(溶液具有均一性),其质量分数=![]() ;
;
(5)加入硝酸银溶液的过程中,溶质是由氯化钡变为硝酸钡,根据两者在反应中的质量关系(208和261),可知,氯化钡的质量由2. 08g减少至0g,硝酸钡的质量由0g增加至2.61g;
(6)根据溶液的均一性,混合物物溶解后所得溶液的质量分数为20.8%,则水的质量分数为1-20.8%=79.2%。
设:样品中BaCl2的质量为A。
则有:![]() A=10.4g;
A=10.4g;
a+39.6ga=10.4g
样品中BaCl2的含量=![]() 。
。

【题目】小明同学对家中久置的袋装固体食品防腐剂的成分产生了兴趣(品名和成分如图所示),于是和同学一起,设计实验进行探究:

[提出问题]久置固体食品防腐剂的成分是什么?
[查阅资料]铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
[作出猜想]久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3 。
[实验探究]甲同学的探究方案如下表:
实验操作 | 实验现象 | 实验结论 |
(1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红。 | 固体中一定含有_____和氢氧化钙。此过程的化学方程式_____。 |
(2)另取少量固体放于试管中,滴加足量的稀盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液。 | 固体中一定含有Fe,一定不含 Fe2O3 |
(3)将步骤(2)中产生的气体通入到澄清的石灰水中 | _____。 | 固体中一定含有CaCO3 |
[交流与反思]
(1)“504双吸剂”中的铁粉可以吸收空气中的_____、_____。
(2)实验操作(2)的实验现象里“有大量无色气体产生”,根据甲同学的整体探究方案推测,无色气体的成分应当是_____、_____。
(3)小明同学认为久置固体食品防腐剂中是否含Fe还可以用_____检验。
(4)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是_____。
(5)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是_____。
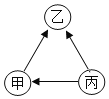
【题目】某校化学研究性学习小组探究气体制取的实验原理与方法.
(1)甲同学将课本的基础知识进行整理如图,请你帮助他完成相关内容.

制取气体 | 所需要品 | 装置连接顺序 | 反应的化学方程式 |
二氧化碳(干燥) | 大理石和稀盐酸 | ______________ | ______________________________ |
(2)乙同学设计的实验装置(如图),既可用于制取气体,又可用于验证物质性质.当打开K1、关闭K2时,利用I、Ⅱ装置可直接进行的实验是______________(填序号).

①大理石与稀盐酸反应制取二氧化碳
②锌与稀硫酸反应制取氢气
(3)丙同学认为在不改变I、Ⅱ、Ⅲ装置的仪器及
位置的前提下,该装置可用于过氧化钠(Na2O2)与水反应制取氧气,另一产物为氢氧化钠,则该反应的化学方程式为:______________________________;她的改进措施是_______________________________________________________.
(4)丁同学打开K2、关闭K1,利用I、Ⅲ装置来验证生成的二氧化碳中含有水蒸气,此时C中盛放的物质是_______________,可以观察到的现象是________________________________________.
(5)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应)作如下回收处理:
①通过以下四步实验操作回收二氧化锰.正确操作的先后顺序是____________(填写选项序号).
a.烘干b.溶解c.过滤d.洗涤
②用所得氯化钾晶体配制50g质量分数为5%的氯化钾溶液,需要氯化钾的质量为_______g.
③过滤、蒸发时都需用到的仪器是__________(填序号).
A.酒精灯B.烧杯C.玻璃棒D.漏斗E.量筒
(6)小明用6.5g可能含有铜、铝、铁、镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2g氢气,则此锌粉中一定含有的金属杂质是________________.