题目内容
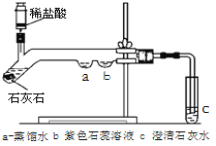
【题目】(9分)为了证明石灰石中含有碳酸盐及探究二氧化碳的性质,某同学设计了如下图所示的实验:

(1)写出石灰石与稀盐酸反应的化学方程式: 。
(2)用注射器注入稀盐酸,一段时间后,可观察到在1、2两处中有一处有明显的现象发生,该实验现象是 。
(3)当观察到现象: , 。证明石灰石中含有碳酸盐。
(4)将燃烧的镁带伸入到盛有二氧化碳的瓶中,发现镁条剧烈燃烧,发出白光,产生一种白色粉末和一种黑色粉末.该反应的化学方程式为: 。
【答案】(1)CaCO3+2HCl==CaCl2+CO2↑+H2O
(2)紫色石蕊试液变红
(3)石灰石表面有气泡产生, 3处石灰水变混浊
(4)2Mg+CO2点燃2MgO + C
【解析】
试题分析:(1)碳酸钙和稀盐酸反应生成的是氯化钙、水和二氧化碳:CaCO3+2HCl==CaCl2+CO2↑+H2O;
(2)二氧化碳能与水反应生成碳酸,碳酸能使紫色的石蕊试液变成红色,故2处的现象是紫色石蕊试液变红;
(3)含有碳酸根离子的物质能与酸法生成二氧化碳,故若看到石灰石表面有气泡产生, 3处石灰水变混浊表示石灰石中含有碳酸根离子;
(4)依据质量守恒定律化学反应前后元素的种类不变,故镁与二氧化碳反应应生成的是白色的氧化镁和黑色的碳:2Mg+CO2点燃2MgO + C。

练习册系列答案
相关题目