题目内容
元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分.
(1)请从上表中查出地壳中含量最多的金属元素的相对原子质量为 .
(2)表中不同种元素最本质的区别是 (填序号):
A.相对原子质量不同 B.质子数不同 C.中子数不同
(3)根据表中的内容总结出一条元素周期表中各元素的排列规律 .
(4)如图是五种粒子的结构示意图
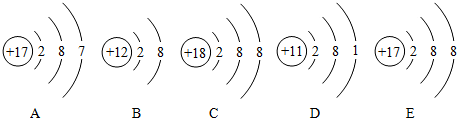
①图中粒子共能表示 种元素.A所表示的元素于 元素(填金属或非金属).
②图中表示的阳离子的是 (用序号表示).
③图中表示的阳离子和阴离子形成化合物是 (填化学式).
| 族 周期 | ⅠA | 0 | ||||||
| 1 | 1H 1.008 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 2He 4.003 |
| 2 | 3Li 6.991 | 4Be 9.012 | 5B 10.81 | 6C 12.01 | 7N 14.01 | 8O 16.00 | 9F 19.00 | 10Ne 20.18 |
| 3 | 11Na 22.99 | 12Mg 24.31 | 13Al 26.98 | 14Si 28.09 | 15P 30.97 | 16S 32.06 | 17Cl 35.45 | 18Ar 39.95 |
(2)表中不同种元素最本质的区别是
A.相对原子质量不同 B.质子数不同 C.中子数不同
(3)根据表中的内容总结出一条元素周期表中各元素的排列规律
(4)如图是五种粒子的结构示意图

①图中粒子共能表示
②图中表示的阳离子的是
③图中表示的阳离子和阴离子形成化合物是
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图,元素的概念
专题:化学用语和质量守恒定律
分析:(1)先弄清地壳中含量最多的金属元素,再根据元素周期表的部分内容,查知其相对原子质量;
(2)掌握元素的概念:具有相同核电荷数(核内质子数)的一类原子的总称;
(3)总结归纳是学习化学的一种重要方法:元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律;
(4)根据粒子结构示意图可知:圆圈内数字表示质子数,质子数决定元素种类,根据质子数和核外电子数关系判断是原子还是离子.
(2)掌握元素的概念:具有相同核电荷数(核内质子数)的一类原子的总称;
(3)总结归纳是学习化学的一种重要方法:元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律;
(4)根据粒子结构示意图可知:圆圈内数字表示质子数,质子数决定元素种类,根据质子数和核外电子数关系判断是原子还是离子.
解答:解:(1)先弄清地壳中含量最多的金属元素为铝元素;再根据元素周期表的内容,查知其相对原子质量为26.98;
(2)根据元素的概念,可知表中不同种元素最本质的区别是质子数不同,故选B;
(3)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律:从左到右,各元素原子的电子层数相同;从左到右,各元素原子的原子序数依次增加;
(4)①由元素的定义可知,质子数决定元素的种类.由原子的结构示意图可知,图中粒子共有四种质子数,能表示四种元素;由A的结构示意图可知,河内的质子数是17.该元素是氯元素,A所表示的元素属于非金属元素.
②由于阳离子的质子数大于核外的电子数,所以,图中表示的阳离子的是B.
③B是镁离子,由于阴离子的质子数小于核外的电子数,所以,由E微粒的结构示意图可知,核内质子是17,核外的电子数是18,E为阴离子,是氯离子,镁离子和氯离子组成的化合物是氯化镁.
故答案为:(1)26.98;(2)B;(3)从左到右,各元素原子的电子层数相同;(4)①四,非金属;②③B;(3)MgCl2.
(2)根据元素的概念,可知表中不同种元素最本质的区别是质子数不同,故选B;
(3)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律:从左到右,各元素原子的电子层数相同;从左到右,各元素原子的原子序数依次增加;
(4)①由元素的定义可知,质子数决定元素的种类.由原子的结构示意图可知,图中粒子共有四种质子数,能表示四种元素;由A的结构示意图可知,河内的质子数是17.该元素是氯元素,A所表示的元素属于非金属元素.
②由于阳离子的质子数大于核外的电子数,所以,图中表示的阳离子的是B.
③B是镁离子,由于阴离子的质子数小于核外的电子数,所以,由E微粒的结构示意图可知,核内质子是17,核外的电子数是18,E为阴离子,是氯离子,镁离子和氯离子组成的化合物是氯化镁.
故答案为:(1)26.98;(2)B;(3)从左到右,各元素原子的电子层数相同;(4)①四,非金属;②③B;(3)MgCl2.
点评:了解元素周期表的特点及其应用;核外电子在化学反应中的作用;了解地壳中元素的分布与含量;了解原子结构示意图与离子结构示意图的特点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列反应既属于化合反应,又属于氧化反应的是( )
A、镁+氧气
| ||
| B、二氧化碳+水→碳酸 | ||
C、碳酸钙
| ||
D、石蜡+氧气
|
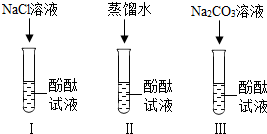 张宁和刘明同学学习完酸、碱、盐后发现:碱溶液能使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红.通过学习知道,碱溶液使酚酞溶液变红,是因为碱在水中离解出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞溶液变红呢?请你帮助他俩完成实验探究.
张宁和刘明同学学习完酸、碱、盐后发现:碱溶液能使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红.通过学习知道,碱溶液使酚酞溶液变红,是因为碱在水中离解出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞溶液变红呢?请你帮助他俩完成实验探究.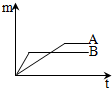 将质量相等的A、B两块金属,分别放入同种的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系如图所示(产物中A、B两种元素的化合价相同).
将质量相等的A、B两块金属,分别放入同种的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系如图所示(产物中A、B两种元素的化合价相同).