题目内容
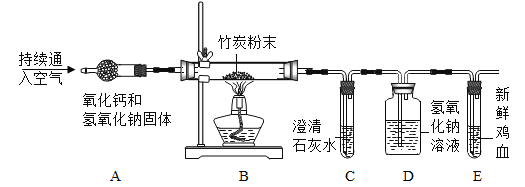
【题目】下图是实验室制取气体的部分装置,请你根据要求回答问题。
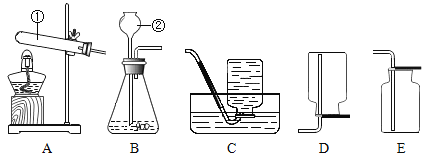
(1)写出标有①.②的仪器名称:①_____;②_____。
(2)写出用大理石和稀盐酸制备二氧化碳的化学方程式_____,发生装置是_____(填编号,下同),收集装置是_____。二氧化碳气体验满的方法是_____。
(3)加热氯酸钾和二氧化锰的混合物来制取并收集氧气的装置是_____,反应的化学方程式是_____。
【答案】试管 长颈漏斗 ![]() B E 将燃着的木条放在集气瓶口,木条熄灭,说明已经集满 AC或AE
B E 将燃着的木条放在集气瓶口,木条熄灭,说明已经集满 AC或AE 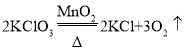
【解析】
(1)仪器①为试管;仪器②为长颈漏斗;
(2)大理石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为:![]() ;该反应属于固液不加热反应,故发生装置应选B;
;该反应属于固液不加热反应,故发生装置应选B;
二氧化碳能溶于水,密度比空气大,应用向上排空气法收集,故收集装置应选E;
二氧化碳气体验满的方法:将燃着的木条放在集气瓶口,木条熄灭,说明已经集满;
(3)加热氯酸钾和二氧化锰的混合物来制取氧气,属于固体加热反应,发生装置应选A,氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集,收集装置应选C或E,故装置应选AC或AE;
该反应的化学方程式为: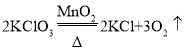 。
。

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
【题目】某研究性学习小组欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品5g,把60g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的杂质不溶于水,也不与稀盐酸反应)。
实验次数 | 1 | 2 | 3 | 4 |
加入稀盐酸的质量/g | 15 | 15 | 15 | 15 |
剩余固体的质量/g | 3.50 | 2.00 | 0.7 | 0.7 |
(1)石灰石样品中碳酸钙的质量分数是多少___________?
(2)求原60g稀盐酸中溶质质量分数___________。