题目内容
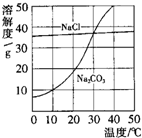 如图为氯化钠、碳酸钠在水中的溶解度曲线.请回答下列问题:
如图为氯化钠、碳酸钠在水中的溶解度曲线.请回答下列问题:(1)10℃时,碳酸钠的溶解度为
10
10
g;(2)20℃时,氯化钠的溶解度
>
>
碳酸钠的溶解度(填写“>”、“<”或“=”);(3)将30℃时氯化钠和碳酸钠两种相同质量的饱和溶液,分别冷却到10℃,析出晶体多的物质是
碳酸钠(或Na2CO3)
碳酸钠(或Na2CO3)
.分析:(1)根据溶解度的识别方法考虑;(2)根据溶解度的大小比较方法考虑;(3)根据降温后溶解度减小的大小考虑.
解答:解:(1)从10℃向上作垂线与碳酸钠曲线的交点,再向纵坐标作垂线对应的数值,所以碳酸钠的溶解度是10g;
(2)从20℃向上做垂线,与曲线的交点在上面的溶解度就大,所以20℃时它们的溶解度大小顺序是:氯化钠的溶解度大于碳酸钠的溶解度;
(3)降温后溶解度减小的多的析出的晶体就多,由图示可知将30℃时氯化钠和碳酸钠两种相同质量的饱和溶液,分别冷却到10℃,碳酸钠的溶解度减小的多,所以析出的多.
故答案为:(1)10;(2)>;(3)碳酸钠(或Na2CO3).
(2)从20℃向上做垂线,与曲线的交点在上面的溶解度就大,所以20℃时它们的溶解度大小顺序是:氯化钠的溶解度大于碳酸钠的溶解度;
(3)降温后溶解度减小的多的析出的晶体就多,由图示可知将30℃时氯化钠和碳酸钠两种相同质量的饱和溶液,分别冷却到10℃,碳酸钠的溶解度减小的多,所以析出的多.
故答案为:(1)10;(2)>;(3)碳酸钠(或Na2CO3).
点评:解答本题关键是要知道溶解度的查法,知道溶解度大小的比较方法,不管是降温还是升温,只要溶解度减小了,饱和溶液就会析出晶体,减小的越多,析出的晶体就越多.

练习册系列答案
相关题目
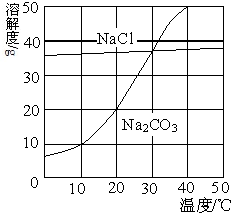
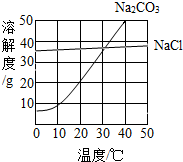 (2013?佛山)如图为氯化钠、碳酸钠在水中的溶解度曲线.请回答下列问题;
(2013?佛山)如图为氯化钠、碳酸钠在水中的溶解度曲线.请回答下列问题;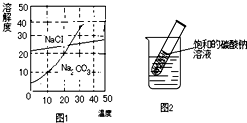 如图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线.
如图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线.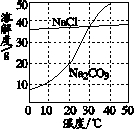 如图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线,请回答问题.
如图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线,请回答问题.