题目内容
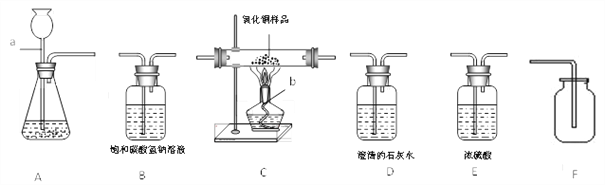
【题目】如下图是CO与氧化铁的反应的实验装置图,请根据图示回答下列问题:
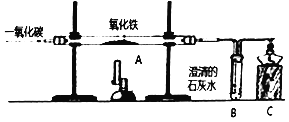
(1)开始实验时,要先通一段时间的一氧化碳后才能点燃A处的酒精喷灯,其目的是_____.
(2)A处观察到的现象是_____,发生反应的化学方程式为_____.
(3)C处可观察到的现象是_____,发生反应的化学方程式为_____.
【答案】 将装置内的空气排出,避免加热时发生爆炸 红棕色粉末变为黑色 Fe2O3+3CO![]() 2Fe+3CO2 产生蓝色火焰 2CO+O2
2Fe+3CO2 产生蓝色火焰 2CO+O2![]() 2CO2.
2CO2.
【解析】(1)由于一氧化碳是可燃性的气体,与空气的混合气体点燃时易发生爆炸,所以开始实验时,要先通一段时间的一氧化碳后才能点燃A处的酒精喷灯,其目的是将装置内的空气排出,避免加热时发生爆炸;(2)在高温条件下在高温时一氧化碳具有还原性,能将氧化铁还原为铁同时生成了二氧化碳,所以A处观察到的现象是红:棕色粉末变为黑色,发生反应的化学方程式为Fe2O3+3CO![]() 2Fe+3CO2;(3)由于尾气中含有一氧化碳能污染空气,在点燃时能燃烧生成了二氧化碳,所以C处可观察到的现象是:产生蓝色火焰,发生反应的化学方程式为:2CO+O2
2Fe+3CO2;(3)由于尾气中含有一氧化碳能污染空气,在点燃时能燃烧生成了二氧化碳,所以C处可观察到的现象是:产生蓝色火焰,发生反应的化学方程式为:2CO+O2![]() 2CO2。
2CO2。

【题目】木炭还原氧化铜得到的红色固体是否全部是铜?
[查阅资料]
(1)铜有+1和+2价两种化合价;
(2)C也能将CuO还原为红色固体Cu2O ;
(3)Cu2O + H2SO4 ===== Cu + Cu SO4 + H2O ;
(4)Cu SO4溶液为蓝色。
[猜想] (1)红色固体只是Cu ;(2)红色固体只是Cu2O ;(3)红色固体是____________。
[实验探究]
实验操作 | 实验现象 | 实验结论 |
取3.6g红色固体放入烧杯中,向其中加入足量的稀硫酸充分反应后,静置。 | 若_______________ | 证明猜想(1)正确 |
若_______________ | 证明红色固体中肯定含有____________________ 可能含有_____________ |
为了进一步确定可能含有的物质是否存在,小华将反应后的液体过滤,将滤渣洗涤、干燥,称得其质量为3.5g ,根据上述数据判断猜想__________(填序号)正确。