题目内容
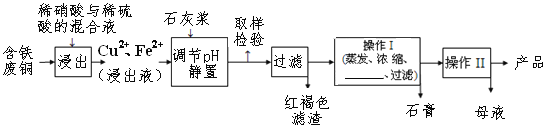
【题目】硫酸铜是一种应用极其广泛的化工原料,易溶于水而不易溶于酒精;铜离子完全沉淀的pH是5左右,铁离子完全沉淀的pH是2左右.以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2O)和副产物石膏(CaSO4·2H2O)的生产流程示意图:
胆矾和石膏在不同温度下的溶解度(g/100g水)如表。
温度(℃) | 20 | 40 | 60 | 80 | 100 |
石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
(1)红褐色滤渣的主要成分是____________;
(2)石灰浆调pH大约要调节到__________
A. 2 B. 5 C. 7 D.10
(3)含铁的废铜和稀硫酸反应的化学方程式________________________________;
(4)操作I最后温度应该控制在___________℃左右;
(5)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、__________、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是_________________。
【答案】 Fe(OH)3 A Fe+ H2SO4 == FeSO4 + H2↑ 100 冷却结晶 减少晶体溶解
【解析】(1)由工艺流程图转化关系可知,浸出液中加入石灰浆调节pH值,铁离子转化为Fe(OH)3沉淀析出,红褐色滤渣的主要成分为Fe(OH)3,(2)由题中信息可知:铜离子完全沉淀的pH是5左右,铁离子完全沉淀的pH是2左右,石灰浆调pH大约要调节到2,使铁离子沉淀,铜离子以溶液存在;(3)含铁的废铜和稀硫酸反应的化学方程式Fe+ H2SO4 == FeSO4 + H2↑;(4)操作I最后温度应该控制在100℃左右,以减少溶液中的杂质,增大硫酸铜的浓度,有利于降温结晶;
(5)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、降温结晶、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是减少晶体溶解,增大硫酸铜晶体的产率。

 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
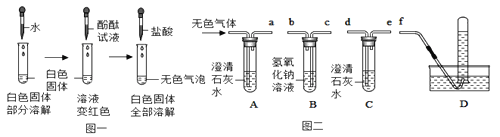
天天向上课时同步训练系列答案【题目】实验室部分装置如下图所示,回答下列问题。

(1)下表是初中几种常见气体的实验室制法,请你在横线上的空白处填上答案。
反应物 | 制取气体 | 发生装置(填字母) | 收集装置(填字母) |
大理石和稀盐酸 | CO2 | B或__________ | _________ |
锌粒和稀硫酸 | _______ | B | F或___________ |
高锰酸钾 | O2 | A | D或___________ |
(2)用C装置制取气体时,如果在反应发生时关上开关,能观察到的现象是:_____________________。
(3)实验室用过氧化氢制取氧气的化学方程式为:________________________________。如果要制取1.6g氧气,需要5%的过氧化氢溶液的质量为:__________g。