题目内容
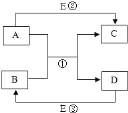
【题目】如图是实验室常用的实验仪器与装置,根据所学化学知识回答下列问题:
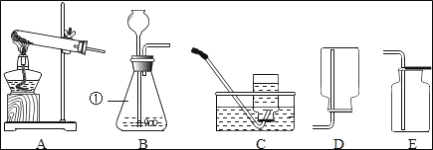
(1)写出标号①的仪器名称___.
(2)写出用A装置制取氧气的一个化学方程式___.
(3)用E装置收集CO2时,检验CO2是否收集满的方法是___.
(4)常温下,乙炔是一种无色气体,密度比空气略小,难溶于水.实验室常用碳化钙固体与饱和食盐水反应来制取乙炔.现选择合适的装置来制取并收集乙炔,应该选择的发生装置是___(填序号,下同),收集装置是___.
【答案】(1)锥形瓶(2)2KClO3![]() 2KCl+3O2↑(3)将燃烧着的木条放在集气瓶口(4)B C
2KCl+3O2↑(3)将燃烧着的木条放在集气瓶口(4)B C
【解析】
(1)熟悉常见仪器,了解它们的名称;
(2)用A装置制取氧气,可用加热高锰酸钾的方法.我们可以根据反应物是高锰酸钾,反应条件是加热.写出化学反应式;
(3)利用二氧化碳不燃烧也不支持燃烧的特点来检验;
(4)根据“实验室常用碳化钙固体与饱和食盐水反应来制取乙炔”.可知是固体和液体在常温下的反应.我们据此选择发生装置.然后根据乙炔密度比空气略小,难溶于水的特点来选择收集装置.
解答:解:(1)熟悉常见仪器,了解它们的名称.图中①是锥形瓶;故答案为:锥形瓶;
(2)如用A装置制取氧气,可用加热高锰酸钾的方法.我们可根据反应物是高锰酸钾和反应条件是加热,写出化学反应式是:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)我们可以利用二氧化碳不燃烧也不支持燃烧的特点,将燃烧着的木条放在集气瓶口,若木条熄灭说明已满.反之,则不满.故答案为:将燃烧着的木条放在集气瓶口;
(4)根据实验室常用碳化钙固体与饱和食盐水反应来制取乙炔.可知是固体和液体在常温下的反应,可选用B装置作为发生装置;又因密度比空气略小,难溶于水.可用排水法收集,故可选C装置作为收集装置.故答案是:B、C.

 智慧小复习系列答案
智慧小复习系列答案【题目】铜镁合金常用作飞机天线等导电材料。欲测定合金的组成(其他元素忽略不计),进行了以下实验:取出3g合金样品,将60g稀硫酸分为6等份依次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
稀硫酸用量 | 第1份 | 第2份 | 第3份 | 第4份 | 第5份 | 第6份 |
剩余固体质量 | 2.5g | m | 1.5g | 1.0g | 0.6g | 0.6g |
(1)铜镁合金属于_____(填“混合物”或“纯净物“);
(2)加入稀硫酸发生反应的化学方程式为_____;
(3)分析数据可知表格中m=_____;
(4)合金样品中铜的质量分数是_____;
(5)若反应过程中产生的气体收集起来,可得到氢气的质量为多少g?_____