题目内容
【题目】现有Mg、C、O2、CO2、Cu(OH)2、H2SO4、Na2CO3、Ca(OH)2 8种物质,选用这8种物质作反应物,按下列要求写出有关的化学反应方程式.
(1)吸热的化合反应:__;
(2)放热的置换反应:__;
(3)需要加热的分解反应:__;
(4)有碱生成的复分解反应:__.
【答案】C+CO2![]() 2CO Mg+H2SO4═MgSO4+H2↑ Cu(OH)2
2CO Mg+H2SO4═MgSO4+H2↑ Cu(OH)2![]() CuO+H2O Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
CuO+H2O Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
【解析】
(1)二氧化碳和碳反应生成一氧化碳是吸热的化合反应:C+CO2![]() 2CO;
2CO;
(2)镁和稀硫酸反应生成硫酸镁和氢气,是放热的置换反应:Mg+H2SO4═MgSO4+H2↑;
(3)氢氧化铜加热生成氧化铜和水,是需要加热的分解反应:Cu(OH)2![]() CuO+H2O ;
CuO+H2O ;
(4)碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,氢氧化钠是碱,是有碱生成的复分解反应:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH 。

 阅读快车系列答案
阅读快车系列答案【题目】西藏“茶马古道”芒康县盐井是香格里拉唯一的产盐区。盐田是用紫红色粘土抹平压实的晒盐池,当地人把卤水注入盐田中经过日晒风吹,就得到上等且味道很好的红盐。为揭密红盐呈红色的原因,实验小组进行了如下探究活动。
(提出问题)红盐中存在什么物质使盐呈现红色?
(查找资料)
1、西藏紫红色粘土中含大量的氧化铁(Fe2O3)。
2、溶液中三价铁离子(Fe3+)遇到硫氰化钾(KSCN)溶液,溶液变为血红色。
(作出猜想)红盐中含少量的氧化铁使盐呈现红色;
(实验探究)小组同学从一定量的红盐中提取少量红色粉末,进行如下实验:
实验操作 | 实验现象 | 实验解释与结论 | |
实验I | 步骤①:取少量红色粉末于试管中,滴加适量稀盐酸; | 红色粉末恰好全部溶解; | 红色粉末中含有_____;步骤①涉及的反应的化学方程式_____ |
步骤②:往①所得溶液中滴入硫氰化钾(KSCN)溶液。 | 溶液变为血红色 | ||
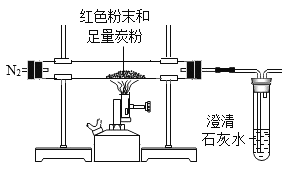
实验Ⅱ | 步骤①:如图所示,将红色粉末与足量的黑色炭粉混合均匀,装入玻璃管中,先通一段时间氮气,再加热。
| 一定时间后,观察到澄清石灰水变浑浊,红色粉末变黑色 | 反应产生的气体为_____;红色粉末中一定含_____元素 |
步骤②:冷却后,取出玻璃管中黑色粉末,将磁铁靠近黑色粉末 | 黑色粉末部分被吸引 | 红色粉末中一定含_____元素 |
(实验结论)猜想_____(填写“正确”或“错误”)。
(实验反思)实验Ⅱ中能否用CO气体代替黑色炭粉并说明理由_____。