题目内容
【题目】元素周期表是化学学习和研究的工具。下图是元素周期表的一部分。
![]()
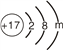
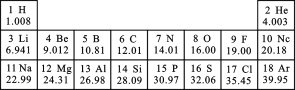
(1)从图6中查出硅元素处于元素周期表中第________主族;
(2)X2+ 与O2-的核外电子排布相同,则X的元素符号是____________,它处于元素周期表中第________周期,它与氧元素组成的化合物的名称________________。
(3)右图中镁元素与氯元素最本质的区别是它们原子中_______________不同;
(4)两种元素具有相似化学性质的组是____________;(填序号)
① Na 、Cl ② O、 S ③ F 、Cl ④ Cl、Ar
(5)若左图表示的是某离子的结构示意图,则m=________。
【答案】 Ⅳ或4 Mg 三 氧化镁 质子数 ②③ 8
【解析】(1)根据从表中可查出硅元素在元素周期表中的信息;
(2)根据离子结构以及元素周期表的信息来分析;
(3)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的是核电荷数(即核内质子数),据此进行分析解答;
(4)根据最外层电子数决定化学性质解答;
(5)若乙表示的是离子,又知为3个电子层,故可知m的值。
解:(1)从表中可查出硅元素处于元素周期表中第Ⅳ或4主族;
(2)O2﹣核外有10个电子,X2+与O2﹣的核外电子排布相同,则X是镁原子,其元素符号为Mg;在元素周期表中位于第三周期,镁元素在化合物中显+2价,氧元素显﹣2价,二者组成的化合物是氧化镁;
(3)元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素的种类得是核电荷数(即核内质子数),故镁元素和氯元素本质的区别是原子的核电荷数(即核内质子数)不同;
(4)最外层电子数相同则化学性质相似,故具有相似化学性质的是②O、S③F、Cl;
(5)若乙表示的是离子,又知为3个电子层,故可知m=8。

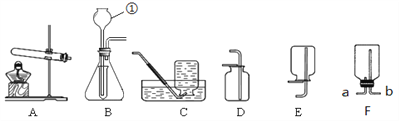
【题目】在学习碳酸钠的化学性质时,甲、乙两位同学分别取20%的碳酸钠溶液和10%的稀盐酸做了如图所示实验。

【实验现象】甲同学的实验中有气泡冒出,乙同学的实验中无气泡冒出。写出甲同学实验的化学方程式___________________。
【提出问题】乙同学的实验中溶液为什么没有明显的现象?
【查阅资料】①碳酸钠和稀盐酸反应仅可以生成二氧化碳,还可以生成碳酸氢钠。
②碳酸钠和氯化钙溶液混合能发生反应,碳酸氢钠和氯化钙溶液混合不发生反应。
【实验设计】证明乙同学所得溶液中含有碳酸钠、碳酸氢钠。
实验步骤 | 实验现象 | 实验结论 |
取适量乙同学实验后的溶液于试管中,加入足量氯化钙溶液 | ___________________ | 乙同学实验溶液中含有碳酸钠和碳酸氢钠 |
取步骤①所得上层清液少量,滴加 _____________________________ | ______________________ |
【实验反思】
(1)碳酸钠和盐酸反应生成物受到盐酸量的影响,稀盐酸_________ (填“过量”或“不足”)时才能有气泡冒出。
(2)当反应物的量不同,生成物可能不同,试另举一例:___________________________。
【注意:若答对以下问题奖励4分,化学试卷总分不超过60分。】
【拓展延伸】欲检验某敞口的试剂瓶中氢氧化钠溶液是否变质,某同学取5ml该液体,滴加少量稀盐酸发现无气泡冒出,证明此氢氧化钠溶液没有变质,同学们认为该结论不合理。 请解释可能的原因为:①_________________________________________;②________________________________________________________________。
为了得到正确的结论,你的改进的方案是___________________________。