��Ŀ����
�ҹ�����ר�Һ�°�ġ������Ƽ��Ϊ�����Ƽҵ������ͻ���Ĺ��ס�����ʳ�Ρ�ˮ��������������̼Ϊԭ�ϣ����Ƶ�̼�����ƺ��Ȼ�泥���������������������Ǽ��������ڲ�ͬ�¶�ʱ���ܽ�ȣ�
|
|
0 |
20 |
40 |
60 |
|
̼������ |
6.9 |
9.6 |
12.7 |
16.4 |
|
�Ȼ��� |
35.7 |
35.8 |
36.6 |
37.3 |
|
�Ȼ�� |
29.4 |
37.2 |
45.8 |
55.2 |
�Ŵӱ������ݿ��Կ������¶ȶ������������ܽ��Ӱ�첻��
��Ҫʹ�Ȼ�隣�����Һ�е��Ȼ�什ᾧ����������������ϸߡ��ϵ͡����¶��½��бȽϺ��ʡ�
��д���������Ƽ����̼�����Ƶķ���ʽ��������������������������������
��������Ϊ�����Ƽ���ŵ����ģ�
A�����������в��ֲ�Ʒ��ѡΪ��ʼԭ��ʹ�á�B������Ʒ��һ�ֿ����õĵ��ʡ���
C����Ӧ����Ҫ���ȡ��� D�������ﲻ�������Ⱦ��������
����Ϊ������ȷ��������������������
�Ȼ��� �ϵ� NH3+H2O+CO2+NaCl= NaHCO3+NH4Cl ABD
�������������������1���ӱ��п��Կ������¶ȶ�NaHCO3��NH4Cl���ܽ�ȵ�Ӱ�춼�Ƚϴ���NaCl���ܽ��Ӱ�첻��ѡ�Ȼ��ơ�
��2�������¶ȵ����ߣ�NH4Cl���ܽ�ȱ�������¶ȱ仯Ӱ��ʿ���ͨ���ڽϸ��¶�������NH4Cl�ı�����Һ��Ȼ���ٽ��£��ᾧ����NH4Cl�İ취��NH4Cl����Һ�з��������
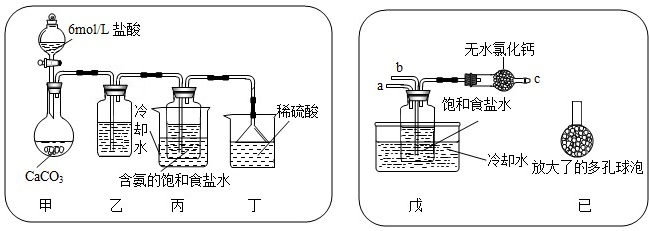
��3�������Ƽ��ԭ���ǣ��Ƚ�����ͨ�뱥��ʳ��ˮ�ж��ɰ���ˮ����ͨ�������̼�����ܽ�Ƚ�С��̼�����Ƴ������Ȼ����Һ���ʻ�ѧ����ʽΪ��NaCl��NH3��H2O��CO2��NaHCO3����NH4Cl
��4�����ݰ���ƴ����ʵ��ԭ�����з�������ʳ�Σ��Ȼ��ƣ���ʯ��ʯ��������������ʯ�ҺͶ�����̼��������Ϊԭ������ȡ�����ʹ����ͨ�뱥��ʳ��ˮ�ж��ɰ���ˮ����ͨ�������̼�����ܽ�Ƚ�С��̼�����Ƴ������Ȼ����Һ����NaCl��NH3��H2O��CO2��NaHCO3����NH4Cl���������ˡ�ϴ�ӵõ���NaHCO3С���壬�ټ��������Ƶô����Ʒ��
A������ʱ�ų��Ķ�����̼����ɻ���ѭ��ʹ�ã������Ȼ�淋���Һ��ʯ�����ϼ��ȣ����ų��İ����ɻ���ѭ��ʹ�ã�����A��ȷ��
B������Ʒ���Ȼ�泥����к��е�Ԫ�أ���һ�ֵ��ʣ�����B��ȷ��
C��̼�����Ʒֽ��ƴ���ʱ��Ҫ���ȣ�����C����
D���Ȼ����һ�ֵ��ʣ��������ã�������Ⱦ�������ȷ����ѡABD
���㣺���⿼�鴿�����ȡ�������ܽ�ȵ�Ӱ�����أ��ᾧ��ԭ������������Ӧ��
������������һ����Ϣ�����⣬����Ϣ�����������ӹ������õ����������ǽ�����Ⱦ���������ƽʱѧϰʱҪ��ǿѵ����

 ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д� С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д�