题目内容
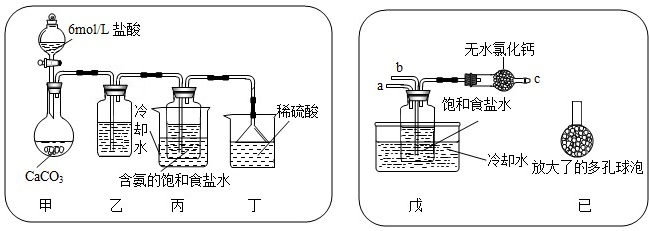
7、我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献.他以食盐、水、氨气、二氧化碳为原料,先制得碳酸氢钠和氯化铵,进而生产出纯碱.下表是几种物质在不同温度时的溶解度:
(1)从表中数据可以看出,温度对
(2)要使NH4Cl饱和溶液中的NH4Cl结晶析出,在
(3)“侯氏制碱法”制NaHCO3的方程式是NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl,该反应能进行的原因是
(1)从表中数据可以看出,温度对
NaCl
的溶解度影响不大.(2)要使NH4Cl饱和溶液中的NH4Cl结晶析出,在
较低
(填“较高”或“较低”)温度下进行比较合适.| 0℃ | 20℃ | 40℃ | 60℃ | |
| NaHC03 | 6.9 | 9.6 | 2.7 | 6.4 |
| NaCl | 35.7 | 35.8 | 6.6 | 37.3 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 |
有溶解度较小的NaHCO3产生
.分析:(1)根据表中氯化钠溶解度随温度变化的情况回答.
(2)根据表中氯化钠溶解度随温度变化的情况回答.
(3)根据表中碳酸氢钠在低温下溶解度很小,易结晶析出,形成沉淀物的特点回答.
(2)根据表中氯化钠溶解度随温度变化的情况回答.
(3)根据表中碳酸氢钠在低温下溶解度很小,易结晶析出,形成沉淀物的特点回答.
解答:解:(1)从表中可以看出,温度对NaHCO3和NH4Cl的溶解度的影响都比较大,对NaCl的溶解度影响不大.
(2)随着温度的升高,NH4Cl的溶解度变大,且受温度变化影响大,可以通过在较高温度下配置NH4Cl的饱和溶液,然后再降温结晶析出NH4Cl的办法将NH4Cl从溶液中分离出来.
(3)NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl这个反应能够进行,是因为NaHCO3在水中的溶解度较小,可以结晶析出,相当生成了沉淀,符合复分解反应的基本条件.
故答案为:(1)NaCl;
(2)较低;
(3)有溶解度较小的NaHCO3产生.
(2)随着温度的升高,NH4Cl的溶解度变大,且受温度变化影响大,可以通过在较高温度下配置NH4Cl的饱和溶液,然后再降温结晶析出NH4Cl的办法将NH4Cl从溶液中分离出来.
(3)NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl这个反应能够进行,是因为NaHCO3在水中的溶解度较小,可以结晶析出,相当生成了沉淀,符合复分解反应的基本条件.
故答案为:(1)NaCl;
(2)较低;
(3)有溶解度较小的NaHCO3产生.
点评:学来源于生产、生活,又服务于生产、生活,氨碱工业是初中化学重要的应用之一,是考查重点,常涉及化学方程式的书写,二氧化碳和氨气通入的顺序及原因,反应时析出碳酸氢钠的原因与物质溶解度的关系等重点内容.

练习册系列答案
相关题目