题目内容
【题目】铁是一种常见的金属,在化学实验以及生活中随处可见它的影子。
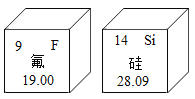
(1)蔚县打树花已经成为一项非常著名的民俗活动。表演者将熔化的铁水泼洒到古城墙上,迸溅形成万朵火花。铁燃烧的生成物化学式为:_______。

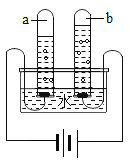
(2)下图是课本中探究铁生锈条件的实验,在甲、乙两图实验中控制的变量是:______。在铁制品表面刷上一层漆,就可以防止生锈,其原因是______。

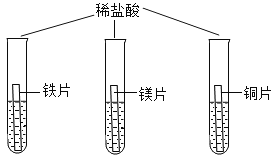
(3)在三个试管中分别加入铁片、镁片、铜片,再分别加入相同质量的稀盐酸,可观察到的实验现象为:________。铁与稀盐酸反应的化学方程式为:_______。
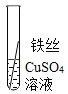
(4)将铁丝放置于硫酸铜溶液中,可观察到溶液变成浅绿色,有红色固体出现,则该反应的化学方程式为:______;它的化学反应基本类型是:_____。
【答案】Fe3O4 空气中的氧气 阻止金属与空气中的氧气、水分等发生反应 铁片、镁片表面有气产生,铜片没有 Fe+2HCl=FeCl2+H2↑ Fe+CuSO4=FeSO4+Cu 置换反应
【解析】
(1)铁燃烧生成四氧化三铁,表示为Fe3O4;
(2)图示实验中,甲中的铁钉既与氧气接触接触,又与水接触,发生了锈蚀;乙中的铁钉只与水接触,没有与氧气接触,没有锈蚀,所以在甲、乙两图实验中控制的变量是氧气;在铁制品表面刷上一层漆,就可以隔绝铁与氧气、水的接触,可以防止生锈;
(3)三种金属的活动性顺序为镁>铁>H>铜,所以在三个试管中分别加入铁片、镁片、铜片,再分别加入相同质量的稀盐酸,可观察到镁片表面快速产生大量的气泡,铁片表面缓慢产生气泡,铜片表面无变化,铁与盐酸反应生成氯化亚铁和氢气化学方程式为:Fe+2HCl=FeCl2+H2↑;
(4)铁比铜活泼,所以铁能与硫酸铜反应生成铜和硫酸亚铁,化学方程式为:Fe+CuSO4=Cu+FeSO4,该反应是由一种单质与一种化合物反应生成另一种单质与另一种化合物,属于置换反应。

 目标测试系列答案
目标测试系列答案【题目】生活中经常遇到一些“长相”类似的物质,如家庭制作食品用到的碳酸钠和碳酸氢钠。区分二者,比较简单的方法就是溶解度法(溶解度曲线见图)。

①小亮同学利用这种方法,在室温条件下设计了下面实验,请完善实验内容:
实验步骤 | 现象和结论 |
取两只试管,各倒入10g水,分别向两试管中逐步加入碳酸钠和碳酸氢钠固体,充分振荡、静置、观察现象。 | 至固体不能再溶解为止,其中,固体溶解量少的,所对应的物质是 ______ (填化学式,下同),另一种物质是 ______ |
②现有碳酸钠(2g)、碳酸氢钠(2g)和足量蒸馏水。请仿照上述①中的方法和实验设计,在室温条件下,调整变量、自主设计实验,进一步区分碳酸钠、碳酸氢钠两种物质:
实验步骤 | 现象和结论 |
______ | ______ |