��Ŀ����
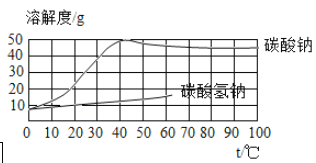
����Ŀ�������о�������һЩ�����������Ƶ����ʣ����ͥ����ʳƷ�õ���̼���ƺ�̼�����ơ����ֶ��ߣ��Ƚϼķ��������ܽ�ȷ����ܽ������ͼ����
��С��ͬѧ�������ַ��������������������������ʵ�飬������ʵ�����ݣ�
ʵ�鲽�� | ����ͽ��� |
ȡ��ֻ�Թܣ�������10gˮ���ֱ������Թ�������̼���ƺ�̼�����ƹ��壬��������á��۲����� | �����岻�����ܽ�Ϊֹ�����У������ܽ����ٵģ�����Ӧ�������� ______ ���ѧʽ����ͬ������һ�������� ______ |
������̼���ƣ�2g����̼�����ƣ�2g������������ˮ��������������еķ�����ʵ����ƣ������������£������������������ʵ�飬��һ������̼���ơ�̼�������������ʣ�
ʵ�鲽�� | ����ͽ��� |
______ | ______ |
���𰸡�NaHCO3 Na2CO3 ȡ��֧�Թܣ��ֱ����2g̼���ƺ�̼�����ƣ��ֱ�����֧�Թ��м�������ˮ����������á��۲����� ������ȫ���ܽ⣬��������ˮ��ģ���̼�����ƣ���������ˮ�ٵģ���̼����
��������
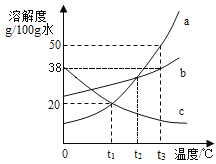
�ٸ����ܽ�����߿�֪�������������£�̼���Ƶ��ܽ�ȱ�̼�����Ƶ��ܽ�ȴ�ȡ��ֻ�Թܣ�������10gˮ���ֱ������Թ�������̼���ƺ�̼�����ƹ��壬����������岻�����ܽ�Ϊֹ�����У������ܽ����ٵ�����Ӧ��������̼�����ƣ���һ��������̼���ƣ��仯ѧʽ�ֱ���NaHCO3��Na2CO3��
����ͬ�����������ʣ��ܽ��С��������ȫ�ܽ����ĵ�ˮ�࣬�ܽ�ȴ��������ȫ�ܽ����ĵ�ˮ�١�ȡ��֧�Թܣ��ֱ����2g̼���ƺ�̼�����ƣ��ֱ�����֧�Թ��м�������ˮ����������á��۲�����������ȫ���ܽ⣬��������ˮ��ģ���̼�����ƣ���������ˮ�ٵģ���̼���ơ�

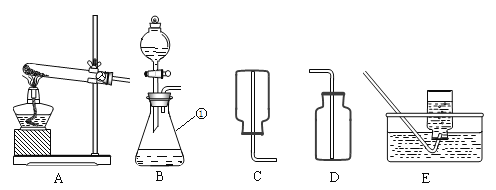
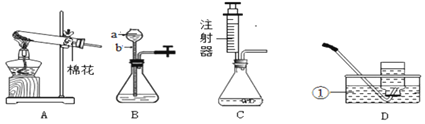
����Ŀ��ͬѧ����ѧϰ��Ļ�ѧ����ʱ����������ͼ��ʾ��ʵ�飮
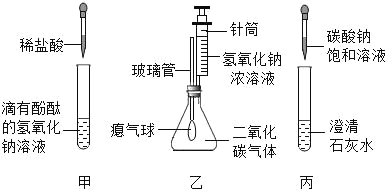
��1���ֱ�д���ס��ҡ���ʵ���з�����Ӧ�Ļ�ѧ����ʽ��
��_____����_____����_____��
���۵ĽǶȿ�������Ӧ��ʵ����_____��
��2����ʵ���еμ�����������Һ�ɹ۲쵽��������_____��
��3����ʵ���й۲쵽�Թ����а�ɫ����������
��4��ʵ�������ͬѧ�ǽ��ס��ҡ�������ʵ��ķ�Һ����ͬһ���ɾ��ķ�Һ���У����տ�����Һ���Dz��ʺ�ɫ���������ʣ�
[�������]��Һ�к�����Щ���ʣ�
[��������]��һ�����е����ʣ�̼��ơ�ָʾ����ˮ��_____��д�������ƣ���
����������ʹ��Һ�ʼ��Ե����ʣ�
��ʹ��Һ�ʼ��Ե�������ʲô��ͬѧ�������²��룮
С����Ϊ��ֻ��̼����
С����Ϊ��ֻ����������
С����Ϊ�����������ƺ�̼����
����Ϊ��������_____��дһ�ֲ��룩��
[ʵ�����]С�������Ȼ�����Һ����֤С�ơ�С�졢С�ֵIJ��룮�������ϻ�Ϥ�Ȼ�����Һ�����ԣ����������ʵ�飮���㽫С����ʵ����Ʋ���������
ʵ������ | Ԥ������ | Ԥ�ƽ��� |
ȡ������Һ�����ϲ���Һ ���Թ��У�������� �Ȼ�����Һ�����ã� | ���а�ɫ��������Һ�ʺ�ɫ�� | _____�IJ�����ȷ�� |
��_____�� | _____�IJ�����ȷ�� | |
��_____�� | _____�IJ�����ȷ�� |
[��˼��չ]�ڷ�����ѧ��Ӧ���������ʵijɷ�ʱ�����˿�����������迼��_____��