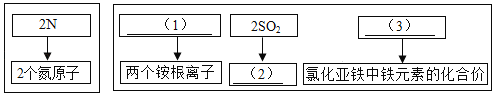
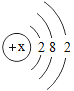题目内容
【题目】建立模型是学习化学的重要方法,下列模型正确的是( )
A.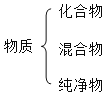 物质分类模型B.
物质分类模型B.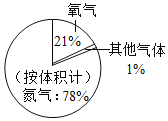 空气组成模型
空气组成模型
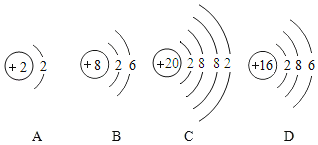
C. 地壳中元素含量模型D.
地壳中元素含量模型D.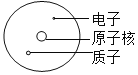 原子结构模型
原子结构模型
【答案】B
【解析】
A、根据纯净物包括化合物和单质分析解答;
B、根据按体积计算空气由78%N2和21%O2还有1%其他成分组成分析解答;
C、根据地壳中元素含量考虑;
D、根据原子核由质子和中子构成分析解答。
A、物质分为纯净物和混合物,纯净物包括化合物和单质,模型中化合物没包括在纯净物中,选项A不正确;
B、按体积计算空气由78%N2和21%O2还有1%其他成分组成,模型描述与事实相符,选项B正确;
C、地壳中元素含量在前五位由多到少的顺序是:氧、硅、铝、铁、钙,选项B不正确;
D、原子核由质子和中子构成,模型中质子不在原子核内,选项D不正确。故选B。

 全能测控期末小状元系列答案
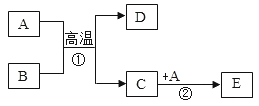
全能测控期末小状元系列答案【题目】小明在课外阅读中得知:氢氧化铜受热会分解生成氧化铜(Ca(OH)2=CuO+X),于是用CuSO4溶液与KOH溶液反应制取氢氧化铜,并对氢氧化铜进行加热。
(1)生成物X的化学式为____。
(2)制取氢氧化铜的化学方程式为____。
(3)小明在加热氢氧化铜时,发现蓝色固体先变成黑色;继续高温灼烧黑色固体变成红色,同时有气体产生。为弄清这种红色固体的成份,进行了如下的探究:
(查阅资料)Cu和Cu2O均为红色固体,且Cu2O+H2SO4=Cu+CuSO4+H2O。
(提出猜想)红色固体是:Ⅰ.Cu;Ⅱ.Cu2O;Ⅲ.①____。
操作 | 现象 | 结论 |
①取灼烧后的红色固体1.44g于试管中,加入足量稀硫酸,加热并充分震荡,静置。 | 溶液由无色变蓝色,固体减少。 | 1.44g红色固体一定有:②____。 |
②过滤、洗涤、干燥。 | 得红色固体 |
(进行实验)
(结论分析)
③据上述实验现象,小明认为猜想Ⅲ正确。但有同学认为小明的判断不严谨,因为猜想___也有相同的现象。
④为了进一步确定1.44g红色固体的成分,同学们将充分反应的固体过滤、洗涤、干燥后称重为1.24g,通过计算后确定猜想Ⅲ正确,请你计算出1.44g红色固体中Cu为____g、Cu2O为______g。
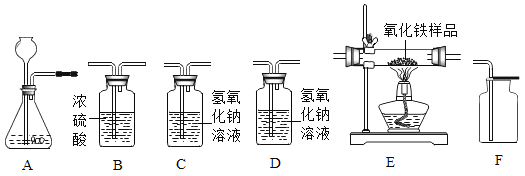
【题目】实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的文字表达式:__________________________
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
(提出猜想)除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
(完成实验)按下表进行实验:并测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度(℃) |
① | 氯酸钾 | 580 |
② | 氯酸钾、二氧化锰(质量比1:1) | 350 |
③ | 氯酸钾、氧化铜(质量比l:1) | 370 |
④ | 氯酸钾、氧化铁(质量比1:1) | 390 |
(分析数据、得出结论)(1)由实验____________与实验④对比,证明猜想合理。
(2)实验所用的三种金属氧化物,催化效果最好的是_____________________。
(反思)(1)若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后质量和__________不变;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证_______________________。
(3)同种催化剂,还有哪些因素可能影响催化效果,请你再探究 (探究一种因素即可)____。