题目内容
【题目】盐通高铁的建成将进一步推动我市经济的发展,在修建铁路的土石方爆破中要用到黑火药,黑火药爆炸时发生反应的化学方程式是2KNO3+3C+S![]() K2S+3CO2↑+X↑,根据以上信息,回答下列问题:
K2S+3CO2↑+X↑,根据以上信息,回答下列问题:
(1)X的化学式是_________。
(2)KNO3中的阴离子是 ________ (填离子符号)。
(3)K2S中硫元素的化合价为 ________ (填序号)。
A.0 B.-2 C.+6 D.+2
(4)黑火药属于_________ (“混合物”或“纯净物”)。
(5)KNO3属于 ________ (填序号)。
A.单质B.化合物C.氧化物D.纯净物
【答案】N2 NO3﹣ B 混合物 BD
【解析】
(1)根据质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式推断生成物X的化学式;
(2)根据离子符号书写方法进行分析;
(3)根据在化合物中正负化合价代数和为零判断;
(4)根据混合物的概念进行分析;
(5)根据物质类别的知识进行分析;
(1)根据反应的化学方程式可知,反应物中S、K、N、O、C原子个数分别为1、2、2、6、3,反应后的生成物中S、K、N、O、C原子个数分别为1、2、0、6、3,根据反应前后原子种类、数目不变,则每个X分子由2个氮原子构成,物质X的化学式为N2;
(2)KNO3中的阴离子是硝酸根离子,离子符号是:NO3﹣;
(3)钾元素显+1价,设:硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x=0,则x=﹣2价,故选B;
(4)根据化学方程式中反应物可知,黑火药中含有多种物质,属于混合物;
(5)KNO3具有固定组成,属于纯净物,是由不同种元素组成的,属于化合物,故选BD。

【题目】蔗糖是生活中常见的一种物质,某兴趣小组对“蔗糖的组成”进行了探究。
(作出猜想)小组同学认为绿色植物通过光合作用将二氧化碳和水转化成葡萄糖和氧气,葡萄糖进一步转化为蔗糖,故蔗糖中一定含有碳、氢元素,可能含有氧元素。
(实验验证)
方案一:小明将蔗糖在氧气中燃烧,检验到生成物中有水和二氧化碳,得出结论“蔗糖是由碳、氢、氧三种元素组成的”。
小刚认为该方案不合理,只能说明蔗糖中一定含有碳、氢元素,不能确定是否含有氧元素,理由是_____。
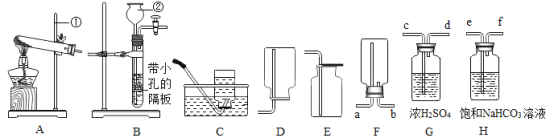
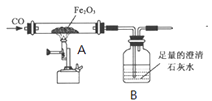
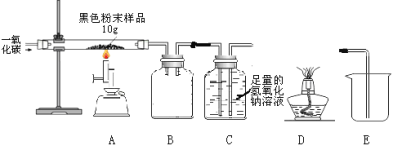
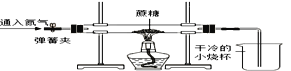
方案二:小刚用上图所示装置进行实验。实验开始先通入一会儿氮气,然后关闭弹簧夹,点燃酒精灯给蔗糖加强热使其发生分解反应。
(1)观察到烧杯内壁_______出现,说明蔗糖中含有氢元素和氧元素。
(2)观察到硬质玻璃管中残留有黑色固体,他猜测该黑色固体是单质碳,另选试剂进行了验证单质碳的实验。实验过程和现象如下:
实验步骤 | 实验现象 |
①、取硬质玻璃管中少量残余黑色固体,放入燃烧匙中点燃,伸入装满氧气的集气瓶中。 ②、燃烧完毕后,向集气瓶中倒入澄清石灰水 | ①黑色固体剧烈燃烧,发出白光; ② ____________________ |
(实验结论)蔗糖是由碳、氢、氧三种元素组成的。
写出上述实验步骤②反应的化学方程式:_________________。
(拓展交流)
(1)方案二中,先通入一会儿氮气的原因______________。
(2)查阅资料得知蔗糖的化学式为C12H22O11。蔗糖分子中氢原子数目是氧原子数目的2倍,但是,蔗糖中氧元素质量却是氢元素质量的8倍。导致出现这种情况的原因_______。