题目内容
(2013?盐城一模)用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新技术.已知获得高铁酸钠的反应为:Fe2O3+mNa2O2=nNa2FeO4+Na2O,下列说法中正确的是( )
分析:A、根据在化合物中元素化合价的代数和为零的原则进行分析判断.
B、根据消毒的作用进行分析判断.
C、根据质量守恒定律:反应前后原子种类和数目均不变,进行分析判断.
D、根据化合物中元素的质量分数=
×100%,进行分析判断.
B、根据消毒的作用进行分析判断.
C、根据质量守恒定律:反应前后原子种类和数目均不变,进行分析判断.
D、根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
解答:解:A、钠元素显+1价,氧元素显-2价,设Na2FeO4中铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则x=+6价,故选项说法正确.
B、消毒的作用是除去有害细菌,不是除去水中可溶性杂质,故选项说法错误.
C、根据质量守恒定律,反应前有2个铁原子,2n=2,则n=2;钠的原子个数为2×2+2=6个,2m=6,m=3;m与n不相等,故选项说法错误.
D、高铁酸钠中钠原子的相对原子质量之和为23×2=46,铁原子的相对原子质量之和为56,氧原子的相对原子质量之和为16×4=64,氧元素的相对原子质量之和最大,则氧元素的质量分数最大,故选项说法错误.
故选A.
B、消毒的作用是除去有害细菌,不是除去水中可溶性杂质,故选项说法错误.
C、根据质量守恒定律,反应前有2个铁原子,2n=2,则n=2;钠的原子个数为2×2+2=6个,2m=6,m=3;m与n不相等,故选项说法错误.
D、高铁酸钠中钠原子的相对原子质量之和为23×2=46,铁原子的相对原子质量之和为56,氧原子的相对原子质量之和为16×4=64,氧元素的相对原子质量之和最大,则氧元素的质量分数最大,故选项说法错误.
故选A.
点评:本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、质量守恒定律、有关化学式的计算等是正确解答本题的关键.

练习册系列答案
相关题目
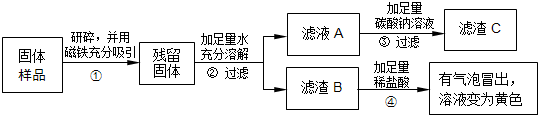
 (2013?盐城一模)红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
(2013?盐城一模)红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.