题目内容
(2013?盐城一模)现有如图所示实验装置,请回答下列问题:

(1)图中e、f仪器的名称:e
(2)用高锰酸钾制氧气,选用的发生装置是
(3)用块状固体和液体常温下制取气体时,用C装置的优点是可以将固液随时分离,能控制反应的发生与停止,对固体药品的要求是
(4)实验室里用过氧化氢溶液和二氧化锰反应制氧气反应的化学方程式为

(1)图中e、f仪器的名称:e
试管
试管
,f长颈漏斗
长颈漏斗
.(2)用高锰酸钾制氧气,选用的发生装置是
A
A
(填字母A、B、C、D),反应的化学方程式是2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
.
| ||
(3)用块状固体和液体常温下制取气体时,用C装置的优点是可以将固液随时分离,能控制反应的发生与停止,对固体药品的要求是
块状固体
块状固体
.观察图C装置,气体制取处于进行
进行
(填“进行”或“停止”)中.(4)实验室里用过氧化氢溶液和二氧化锰反应制氧气反应的化学方程式为
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
,反应前后二氧化锰的质量
| ||
不变
不变
(“不变”或“变大”或“变小”).该实验不能
不能
(填“能”或“不能”)选用C装置来控制反应发生或停止.若用D装置来收集生成的氧气,气体应从g
g
(填g或h)通入.分析:(1)依据常用仪器的用途和名称回答;
(2)根据高锰酸钾制取氧气的反应物的状态和反应条件选择发生装置,并据反应原理书写方程式;
(3)根据隔板的特点分析固体的状态;观察固液是接触还是分离判断反应的发生和停止;
(4)用过氧化氢溶液和二氧化锰反应制氧气,同时产生水,写出反应的方程式;根据催化剂的特征分析质量的变化;根据二氧化锰的状态分析装置的使用;根据氧气的密度选择进气口.
(2)根据高锰酸钾制取氧气的反应物的状态和反应条件选择发生装置,并据反应原理书写方程式;
(3)根据隔板的特点分析固体的状态;观察固液是接触还是分离判断反应的发生和停止;
(4)用过氧化氢溶液和二氧化锰反应制氧气,同时产生水,写出反应的方程式;根据催化剂的特征分析质量的变化;根据二氧化锰的状态分析装置的使用;根据氧气的密度选择进气口.
解答:解;(1)e是试管;f是长颈漏斗,故填:试管;长颈漏斗;
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,属于固体加热型,故选发生装置A;反应的方程式是:2KMnO4
K2MnO4+MnO2+O2↑;故填:A;2KMnO4
K2MnO4+MnO2+O2↑;
(3)由于隔板上有孔,便于液体的进入,因此固体应该是块状的,C装置是固液接触的状态,因此反应正在进行;
故填:块状固体;进行;
(4)过氧化氢在二氧化锰的催化下分解产生了水和氧气,其化学方程式为:2H2O2
2H2O+O2↑;二氧化锰作为催化剂,在化学反应前后质量不变;因为二氧化锰是粉末状固体,会从隔板漏下去,因此不能用C装置作为发生装置;因为氧气的密度比空气大,会聚集在集气瓶的下方,因此进气口是长管g;
故答案为:2H2O2
2H2O+O2↑;不变;不能;g.
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,属于固体加热型,故选发生装置A;反应的方程式是:2KMnO4
| ||
| ||
(3)由于隔板上有孔,便于液体的进入,因此固体应该是块状的,C装置是固液接触的状态,因此反应正在进行;
故填:块状固体;进行;
(4)过氧化氢在二氧化锰的催化下分解产生了水和氧气,其化学方程式为:2H2O2
| ||
故答案为:2H2O2
| ||
点评:本题考查了常见气体的制取装置、收集方法等的选择及反应原理的书写,并在此基础上对装置进行评价,关键是明确发生装置、收集方法选择的依据及原理.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
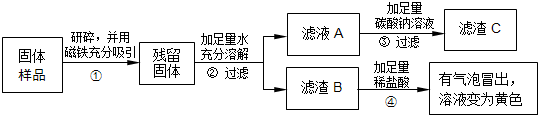
 (2013?盐城一模)红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
(2013?盐城一模)红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.