题目内容
【题目】FeCl3可用作催化剂和外伤止血剂.某实验兴趣小组利用FeCl3腐蚀电路铜板后的溶液(主要成分为FeCl2、CuCl2)进行了氯化铁回收实验.
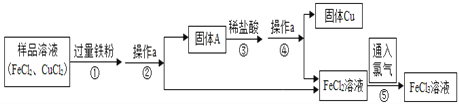
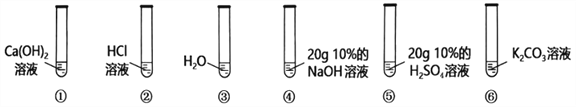
(1)写出步骤①中发生反应的化学方程式是_________.
(2)步骤②中的操作a的名称是___;
(3)固体A的成分是_____________.(填化学式)
(4)步骤⑤反应的基本类型是________,
(5) FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用____(用字母表示)最合理。
A.稀硝酸 B .稀硫酸 C .稀盐酸 D .稀醋酸
【答案】 Fe + CuCl2= Cu +FeCl2 过滤 Fe、Cu 化合反应 C
【解析】(1)铁的金属活动性比铜强,能置换出氯化铜中的铜,生成铜和氯化亚铁;(2)根据分离固体和液体混合物的方法是过滤解答;(3)根据铁能置换出氯化铜中的铜及铁过量解答;(4)根据氯化亚铁和氯气反应生成氯化铁解答;(5)根据盐酸能够和氢氧化铁反应不产生新的杂质,可以防止氯化铁变质产生氢氧化铁解答。(1)铁的金属活动性比铜强,能置换出氯化铜中的铜,生成铜和氯化亚铁,反应的化学方程式为Fe+CuCl2= Cu+FeCl2;(2)步骤②中的操作是分离固体和液体混合物,故步骤②中的操作a的名称是过滤;(3)铁能置换出氯化铜中的铜及铁过量,故固体A的成分是Fe、Cu;(4)步骤⑤发生的反应是氯化亚铁和氯气反应生成氯化铁,符合“多变一”的形式,属于化合反应;(5)盐酸能够和氢氧化铁反应不产生新的杂质,可以防止氯化铁变质产生氢氧化铁,故选C。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案【题目】某泡腾片溶于水时,其成分中碳酸氢钠(NaHCO3)与柠檬酸(C6H8O7,相对分子质量为192)发生反应的原理为:3NaHCO3 + C6H8O7 = Na3C6H5O7 + 3H2O + 3CO2↑。将1片泡腾片(4 g/片)加入盛有足量水的烧杯中,记录烧杯中物质总质量变化如表所示:(假设气体全部扩散,反应物恰好完全反应)
反应时间/min | 0 | t1 | t2 | t3 | t4 |
总质量/g | 250.00 | 249.68 | 249.48 | 249.34 | 249.34 |
根据化学方程式计算:每片泡腾片中柠檬酸的质量分数为______________。