题目内容
【题目】在学习了碳单质的知识后,兴趣小组的同学们用以下实验装置来探究活性炭是否只由碳元素组成。请完成下列各小题:
[查资料]①活性炭能燃烧生成二氧化碳。
②氢氧化钠溶液能吸收二氧化碳。
③图二中产生的二氧化碳全部被氢氧化钠溶液吸收。
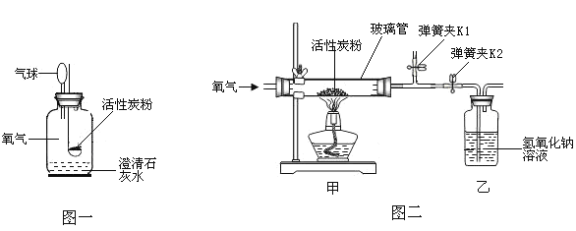
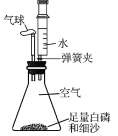
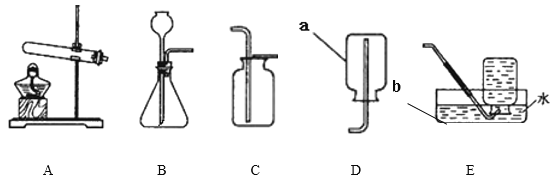
(1)第一小组的同学用图一装置进行探究,他们将活性炭粉点燃后迅速伸入到盛满氧气的集气瓶中燃烧。
①同学们观察到活性炭粉燃烧,发出白光,澄清石灰水变浑浊,写出澄清石灰水变浑浊的化学方程式_____。同学们同时还能观察到的现象是_____。
②图一中气球的作用是_____。
③第一兴趣小组的同学通过图一中澄清石灰水变浑浊分析得出结论:活性炭是只由碳元素组成的。你是否同意这个结论:_____;你的理由是_____。
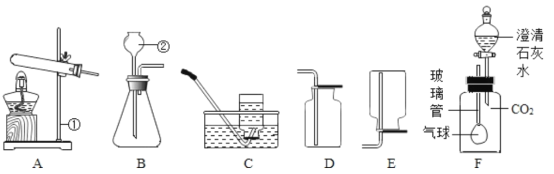
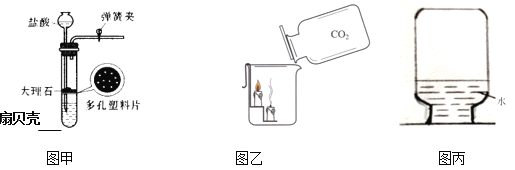
(2)第二小组的同学在老师的指导下用图二装置进行探究,他们用电子天平称量1.2g高纯度活性炭粉,装入玻璃管中,同时称量乙装置的质量。
(3)连接好装置进行实验,先打开弹簧夹K1,关闭弹簧夹K2,缓慢通入氧气,将玻璃管中空气排尽后打开弹簧夹K2,关闭弹簧夹K1;再点燃酒精灯加热。待活性炭粉反应完后继续通入一会氧气。最后再用电子天平称量乙装置的质量,发现乙装置增加了4.4g。
①以上实验中,缓慢通入氧气,将玻璃管中空气排尽后打开弹簧夹K2,关闭弹簧夹K1,请用实验证明玻璃管中空气确实已排尽,你的实验是_____,实验过程中通入氧气要缓慢的一个主要原因是_____。
②开始时为什么是排尽玻璃管中的空气_____,活性炭粉反应完后继续通入一会氧气的原因是_____。
③数据处理:乙装置增加的4.4 g就是甲中活性炭粉燃烧生成的4.4g二氧化碳的质量,请你计算其中碳元素的质量_____。
(4)结论:活性炭只由碳元素组成。
【答案】CO2+Ca(OH)2=CaCO3↓+H2O 气球变小 缓冲作用 不同意 澄清石灰水变浑浊只能证明活性炭中含有碳元素 在K1处放一根带火星的木条,木条复燃,证明空气已排尽 使木炭与氧气充分反应 排除空气中二氧化碳对实验的干扰 使生成的二氧化碳充分被氢氧化钠溶液吸收 1.2g
【解析】
(1)①二氧化碳能和氢氧化钙反应生成碳酸钙沉淀和水,反应的方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;生成的二氧化碳被澄清石灰水吸收,瓶内气压减小,同学们同时还能观察到的现象是:气球变小。
故填:CO2+Ca(OH)2=CaCO3↓+H2O;气球变小;
②图一中气球起到缓冲的作用。故填:缓冲作用;
③澄清石灰水变浑浊只能证明活性炭中含有碳元素,不能证明活性炭是只由碳元素组成的。故填:不同意;澄清石灰水变浑浊只能证明活性炭中含有碳元素。
①检验空气已排尽的方法是:在K1处放一根带火星的木条,木条复燃,证明空气已排尽;实验过程中通入氧气要缓慢的一个主要原因是使木炭与氧气充分反应。故填:在K1处放一根带火星的木条,木条复燃,证明空气已排尽;使木炭与氧气充分反应。
②开始时排尽玻璃管中的空气目的是排除空气中二氧化碳对实验的干扰;活性炭粉反应完后继续通入一会氧气的原因是使生成的二氧化碳充分被氢氧化钠溶液吸收;故填:排除空气中二氧化碳对实验的干扰;使生成的二氧化碳充分被氢氧化钠溶液吸收。
③设活性炭中碳元素的质量为x。

x=1.2g
故填:1.2g;

【题目】学习了碳单质的化学性质,知道碳与氧气反应能够生成CO2或CO后,某学习小组同学联想到木炭粉与氧化铜发生反应可能有:①2CuO+C![]() 2Cu+CO2↑;②CuO+C
2Cu+CO2↑;②CuO+C![]() Cu+CO↑。他们想验证自已的想法,请你同他们一起进行探究。
Cu+CO↑。他们想验证自已的想法,请你同他们一起进行探究。
(猜想与假设)
木炭粉与氧化铜反应生成的产物有三种可能:
(1)产物是铜和一氧化碳;
(2)产物是铜和二氧化碳;
(3)产物是____________________。
(设计方案)
(1)检验产物中是否有CO2的方法是_____________________(用化学方程式表示)。
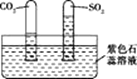
(2)如何检验产物是否存在CO,学习小组同学找查了资料: CO的特征反应是CO能使某种氯化钯的黄色混合液变蓝。
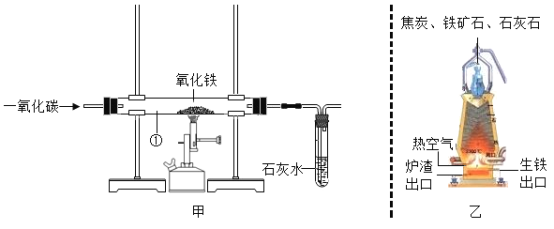
(实验结论)设计的实验装置(如图)
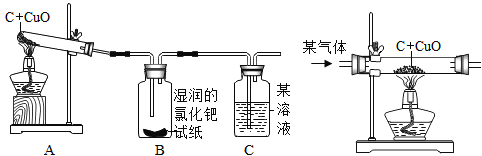
实验报告:
实验现象 | 实验结论 |
①A中________________ | ①有铜生成 |
②B中黄色试纸变蓝 | ②有______________生成 |
③C中_______________ | ③有CO2生成 |
(反思与评价)
(1)实验结束时,为防止Cu被氧化,必须先停止加热,待Cu冷却后再将试管口的胶塞取下,因此,若没有B瓶,可能导致的后果是__________________。
(2)从环保角度看,如图装置有缺陷,怎么办?___________________。
(3)检验生成的气体中是否含有CO,也可以将混合气体通过灼热的氧化铜粉末,看黑色固体是否会逐渐变红,写出相关反应的化学方程式_____________________。
(拓展与延伸)
(1)若采用如图装置代替图中A装置,既可排尽试管中的空气,还可以将反应产生的气体赶出来,那么通入的“某气体”是什么?________________________。
(2)假若24.4g木炭粉与氧化铜混合物充分反应后,只生成二氧化碳气体,且反应后剩余固体质量为20g。求剩余固体中金属铜的质量分数__________________。