题目内容
【题目】碱石灰是实验室中常用的干燥剂。
(查阅资料)①碱石灰是氧化钙、氢氧化钠的固体混合物。
②氯化钙溶液呈中性。
③CaCl2 + Na2CO3 = CaCO3 ↓+ 2NaCl
(提出问题)对实验室中久置的碱石灰样品的成分进行探究。
(进行猜想)久置碱石灰样品中可能含有 CaO、NaOH、Ca(OH)2、Na2CO3、CaCO3 中的两种或两种以上成分。上述五种物质中,属于碱的是_______。样品中可能含有 Ca(OH)2 的原因是(请用化学方程式表示)_______。
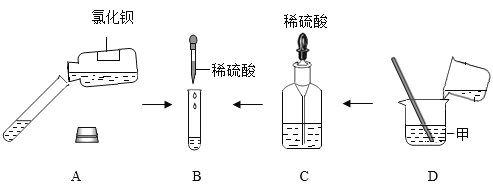
(实验过程)
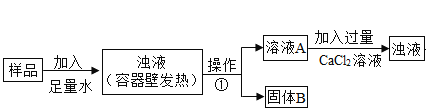
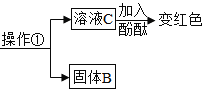
试回答下列问题:
(1)操作①的名称是_______。
(2)根据实验操作及现象,下列说法正确的是_______。
A样品中加水后容器壁发热,说明样品中一定含有 CaO
B样品加足量水后仍有固体,说明样品中一定含有 CaCO3
C溶液 A 加入 CaCl2 溶液后产生固体,说明样品中一定含有 Na2CO3
D溶液 C 加入酚酞变红,说明样品中一定含有 NaOH
(3)向溶液 A 中加入过量的 CaCl2 溶液的操作中,判断加入试剂过量的方案是______。
(4)写出溶液 C 中所含阴离子的符号______。
(实验结论)该久置碱石灰样品中肯定含有的成分是_______,其它成分尚不能确定。
【答案】NaOH、Ca(OH)2 CaO +H2O=Ca(OH)2 过滤 C 取滴加了CaCl2溶液后的浊液的上层清液少许放入试管中,加入Na2CO3溶液,若有白色沉淀产生,则说明加入试剂过量。(反之,则不过量。) OH-、Cl- Na2CO3
【解析】
[进行猜想]
根据碱的定义可以判断氢氧化钠和氢氧化钙为碱;氧化钙与水反应生成氢氧化钙。属于碱的是NaOH、Ca(OH)2;样品中可能含有 Ca(OH)2 的原因是CaO +H2O=Ca(OH)2;
[实验过程]
(1)根据操作后得到是固体和液体,可以知道该操作为过滤;
(2)A、将样品加入水中后得到较热的浊液,能够使浊液温度升高的是氢氧化钠溶于水放热,氧化钙和水反应放热,故两者都有可能,故A错误;
B、如果固体中含有碳酸钠,与氢氧化钙接触会产生沉淀,所以在原混合物中不一定有碳酸钙,故B错误;
C、根据所给的物质中能够和氯化钙产生沉淀只有碳酸钠,故C正确;
D、向溶液C加入酚酞后,酚酞变红,虽然可以证明存在着氢氧根离子,但是由于在向样品中加入足量水后,如果样品中同时存在着碳酸钠和氢氧化钙,那么它们要反应生成氢氧化钠,而在后续的操作中不能排除这个反应的干扰,所以不能确定溶液C中的氢氧化钠是来自于样品中,还是反应生成的,故D错;故选C;
(3)氯化钙与碳酸钠反应生成碳酸钙沉淀和氯化钠。若氯化钙过量则继续滴加碳酸钠溶液会产生白色沉淀,向溶液 A 中加入过量的 CaCl2 溶液的操作中,判断加入试剂过量的方案是取滴加了CaCl2溶液后的浊液的上层清液少许放入试管中,加入Na2CO3溶液,若有白色沉淀产生,则说明加入试剂过量。(反之,则不过量。);
(4)溶液 C加酚酞变红色,酚酞试液只有遇到碱性溶液才会变红,故在溶液中一定存在着氢氧根离子。根据流程可知,溶液一定存在氯离子。溶液 C 中所含阴离子的符号是OH-、Cl-;
[实验结论]根据实验现象加入氯化钙溶液产生了白色沉淀,可以得出在该固体中一定含有碳酸钠。