题目内容
【题目】在反应A+B=C+D中,20g A和10g B恰好完全反应,生成5g C,若要制得5g D,则需要B的质量为( )
A.5g
B.4g
C.2g
D.3g
【答案】C
【解析】解:在反应A+B=C+D中,20g A和10gB恰好完全反应,生成5g C,同时生成D的质量为:20g+10g﹣5g=25g, 即反应中A、B、C、D的质量比是:20:10:5:25,
设若要制得5g D,则需要B的质量为x,
A+ | B=C+ | D |
10 | 25 | |
X | 5g |
![]() =
= ![]() ,
,
x=2g,
故选:C.
【考点精析】本题主要考查了质量守恒定律及其应用的相关知识点,需要掌握①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏才能正确解答此题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】用Ba(OH)2溶液测定某种氮肥中(NH4)2SO4的质量分数(杂质溶于水,但不参加反应).实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入Ba(OH)2溶液,生成气体及沉淀质量与加入Ba(OH)2溶液的质量关系如下所示: 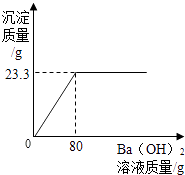
实验次序 | 1 | 2 | 3 |
滴入Ba(OH)2溶液的质量/g | 20 | 40 | 60 |
生成气体的质量/g | 0.85 | m | 2.55 |
试分析并计算:[已知:(NH4)2SO4+Ba(OH)2=BaSO4↓+2H2O+2NH3↑]
(1)表格中m的值为g.
(2)实验所用氢氧化钡溶液中溶质的质量分数.
(3)该氮肥中(NH4)2SO4的质量分数.(计算结果精确至0.1%)