题目内容
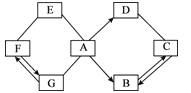
【题目】(某工厂废料中可能含有铜、氧化铜和碳粉中的一种或几种。为确定其成分,设计如下流程并实验。【资料:CuO + H2SO4 = CuSO4 + H2O】

根据流程回答下列问题:
(1)实验操作Ⅰ的名称是_____________。
(2)蓝色溶液B与Fe反应的化学方程式是_______________。
(3)废料的成分是____________。
【答案】(1)过滤(2)Fe+H2SO4=FeSO4+H2↑
Fe+CuSO4=FeSO4+Cu(3)CuO、C、Cu
【解析】
试题分析:(1)铜、氧化铜和碳粉中加入a得到了蓝色溶液,故可知加入的是稀硫酸,稀硫酸与氧化铜反应生成了硫酸铜和水,铜、碳粉均不能与稀硫酸反应,可通过过滤的方法将固体和液体分离;
(2)蓝色溶液中加入铁粉生成了气体,说明加入的稀硫酸是过量的,即蓝色溶液中含有稀硫酸和硫酸铜,加入铁粉后,铁与稀硫酸反应生成硫酸亚铁和氢气,铁还能与硫酸铜反应生成铜和硫酸亚铁:Fe+H2SO4=FeSO4+H2↑ ; Fe+CuSO4=FeSO4+Cu;
(3)固体A在空气中最少不能完全反应,并生成了气体,故固体A中含有碳粉和铜,那么废料中含有三种物质:铜、碳粉和氧化铜。

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目